核磁共振(NMR)技术已广泛应用于复杂分子结构测定和医学诊断等高科技领域。已知只有质子数和中子数均为奇数的原子核有NMR现象。试判断下列原子均可产生NMR现象的是
| A.18O31P119Sn |
| B.27Al19F12C |
| C.80Br2H14N |
| D.元素周期表中第一周期所有元素的原子 |
已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-和CrO42-,浓度均为0.010mol·L-1,向该溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为
| A.Cl-、Br-、CrO42- | B.CrO42-、Br-、Cl- |
| C.Br-、Cl-、CrO42- | D.Br-、CrO42-、Cl- |
常温下,在BaSO4饱和溶液中加入Na2SO4固体,达到溶解平衡时,下列说法正确的是
| A.c (Ba2+) =" c" (SO42-) |
| B.c (Ba2+) 增大,c(SO42-) 减小 |
| C.c (Ba2+) ≠ c (SO42-),c(Ba2+)·c(SO42-) = KSP (BaSO4) |
| D.c (Ba2+) ≠ c (SO42-),c(Ba2+)·c(SO42-) ≠ KSP (BaSO4) |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表: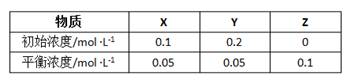
下列说法错误的是
| A.反应达到平衡时,X的转化率为50% |
B.反应可表示为X+3Y 2Z,其平衡常数为1600 2Z,其平衡常数为1600 |
| C.增大压强可使平衡向生成Z的方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
欲测定某氢氧化钠样品中可能的变质成分碳酸钠的含量,张同学取该样品少量放于烧杯中,向其中慢慢滴加10%的稀盐酸,所加盐酸与产生气体的质量关系图如下: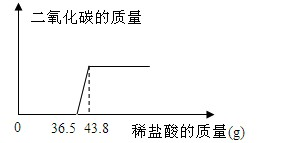
(1)求反应完毕后产生二氧化碳的质量?
(2)原固体中氢氧化钠的质量分数是多少?(结果保留一位小数)
已知Br2+2Fe2+="2Br" -+2Fe3+ , 现向含溶质a mol的FeBr2溶液中通入b mol Cl2,充分反应。下列说法不正确的是
| A.离子的还原性强弱:Fe2+>Br->Cl- |
| B.当氯气少量时,发生的离子反应:2Fe2++Cl2=2Fe3++2Cl- |
| C.当a=b时,反应后溶液的离子浓度:c(Fe3+)︰c(Br-)︰c(Cl-)=1︰2︰2 |
| D.当氯气过量时,发生离子反应:2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |