已知:常温常压下,D、E、F、I、J为气体; 1molE与含1molF的水溶液恰好反应生成B。B是一种常见的化肥。物质 之间有如下图所示转化关系(部分反应中生成的水已略去)。
之间有如下图所示转化关系(部分反应中生成的水已略去)。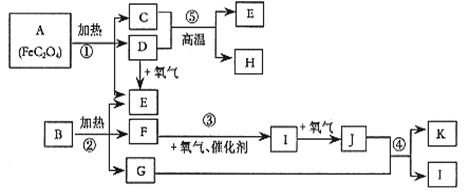
试回答下列问题:
(1)已知A中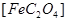 和C中Fe元素均为+2价,则
和C中Fe元素均为+2价,则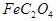 中碳元素的化合价为______
中碳元素的化合价为______
(2)B的化学式为___________________。
(3)写出反应③的化学方程式 _______________________ _____。
(4)写出过量单质H与K的稀溶液反应的离子方程式:_____________________。
(14分)三氯氧磷(化学式:POCl3)常用作半导体掺杂剂及光导纤维原料。氯化水解法生产三氯氧磷的流程如下:
(1)氯化水解法生产三氯氧磷的化学方程式为。
(2)通过佛尔哈德法可以测定三氯氧磷产品中Cl元素含量,实验步骤如下:
Ⅰ.取a g产品于锥形瓶中,加入足量NaOH溶液,待完全水解后加稀硝酸至酸性。
Ⅱ.向锥形瓶中加入0.1000 mol·L-1的AgNO3溶液40.00 mL,使Cl-完全沉淀。
Ⅲ.向其中加入2 mL硝基苯,用力摇动,使沉淀表面被有机物覆盖。
Ⅳ.加入指示剂,用c mol·L-1NH4SCN溶液滴定过量Ag+至终点,记下所用体积。
已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12
①滴定选用的指示剂是(选填字母),滴定终点的现象为。
a.FeCl2 b.NH4Fe(SO4)2 c.淀粉 d.甲基橙
②实验过程中加入硝基苯的目的是,如无此操作所测Cl元素含量将会 __(填“偏大”、“偏小”或“不变”)
(3)氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水。在废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。
①在沉淀前先加入适量漂白粉的作用是。
②下图是不同条件对磷的沉淀回收率的影响图像。
处理该厂废水最合适的工艺条件为(选填字母)。
a.调节pH=9 b.调节pH=10 c.反应时间30 min d.反应时间120 min
③若处理后的废水中c(PO43-)=4×10-7 mol·L-1,溶液中c(Ca2+)=mol·L-1。(已知Ksp[Ca3(PO4)2]=2×10-29)
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下表:
(1)写出两种均含A、B、C、F四种元素的化合物在溶液中相互反应的离子方程式
(2)D、E、F的简单离子半径由大到小的顺序是(直接用化学式表示)。
(3)向Fe和D单质组成的混合物中,加入足量F的最高价氧化物对应水化物的稀溶液,固体全部溶解。向所得的溶液中加入过量的氢氧化钠溶液,将产生的沉淀过滤出来,经洗涤、干燥、灼烧后得到一种固体,经称量发现该固体的质量和原混合物的质量恰好相等。则原混合物中D单质的质量分数为。
(4)一定量的石灰乳中通入一定量的E单质,两者恰好完全反应,生成物中有三种含E元素的离子,其中两种离子的物质的量(n)与反应时间(t)的曲线如图所示。此时反应的化学方程式为。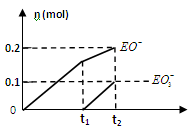
(5)A、B形成的化合物BA在有机合成中用途很广泛。它可以夺取很多化合物中的质子而生成相应的钠的化合物。写出它与乙醇反应的化学方程式。
某化学探究学习小组同学在实验室中配制100mL 0.5mol/L的Na2CO3溶液。
(1)下列实验步骤是配制溶液所必需的步骤,请使用各步骤的编号按照实验操作时的顺序进行排序(填写各步骤的编号)_______________________;
①溶解 ②定容 ③计算 ④转移 ⑤称量 ⑥洗涤并转移 ⑦反复倒转摇匀
(2)实验中除了需要天平、药匙、烧杯、玻璃棒外,还需要的仪器有_______________;
(3)用碳酸钠晶体(Na2CO3·10H2O)配制该溶液需要g,若称取等质量的Na2CO3 ,则所配制溶液的浓度(填写偏高、偏低、无影响);
(4)该小组在实验室中发现了一张注射用质量分数为5%的葡萄糖(分子式为C6H12O6,相对分子质量为180)溶液的标签,如下图所示:
该溶液的物质的量浓度为________(小数点后保留2位数)。
(10分)自然界中的物质多数是以混合物的形式存在,下面是混合物的分离和提纯要求,请填空:
(1)除去NaCl中的Na2SO4,依次加入的溶液为(填溶质化学式):______、______、________;
(2)如图是常用的实验仪器(铁架台和玻璃导管、橡皮管、瓶塞等略去)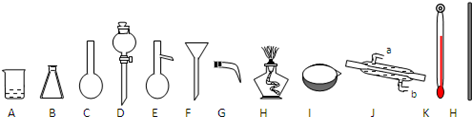
①填写以下仪器的名称:D,J;
②用四氯化碳萃取溴水中Br2单质,萃取能否用酒精代替四氯化碳进行实验?,解释其原因;
③蒸馏装置中,在E中加入沸石的目的是,仪器J的冷凝水应该进出(填写a、b)。
(6分)(1)在标准状况下,有下列物质:①4 g H2 ②33.6 L CH4 ③1 mol H2O ④3.01×1023个O2 ,其中含分子数最多的是(请在横线上填写序号,下同),含原子数最少的是,质量最大的是,体积最小的是;
(2)含0.4 mol Al3+的Al2(SO4)3中所含的SO42一的物质的量是;
(3)若1克H2O中含有a个氢原子,则阿伏加德罗常数用含a的代数式可表示为。