下列事实不能用勒夏特列原理解释的是
| A.用排饱和食盐水法收集Cl2 |
| B.温度控制在500℃有利于合成氨反应 |
| C.打开碳酸饮料会有大量气泡冒出 |
D.工业制钾 Na(l)+KCl(l)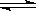 NaCl(l)+K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来 NaCl(l)+K(g)选取适宜的温度,使K成蒸气从反应混合物中分离出来 |
在某容积一定的密闭容器中,可逆反应2A(g)+B(g) xC(g)有如下图(a)、(b)所示的关系曲线,试判断下列对图(b)的说法正确的是()
xC(g)有如下图(a)、(b)所示的关系曲线,试判断下列对图(b)的说法正确的是()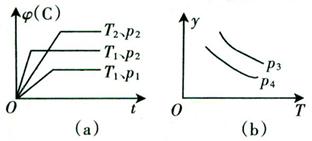
| A.p3<p4,y轴表示A的转化率 |
| B.p3>p4,y轴表示B的转化率 |
| C.p3<p4,y轴表示混合气体的密度 |
| D.p3>p4,y轴表示混合气体中A的浓度 |
奥司他韦是治疗新型甲型H1N1流感的首选药物。其分子式为C16H28N2O4·H3PO4,结构简式如右图所示:

 根据奥司他韦的结构,下列说法正确的是:()
根据奥司他韦的结构,下列说法正确的是:()

A.该物质1mol能与4 mol NaOH反应 |
B.该物质能使溴水褪色,也能和酸性高锰酸钾溶液反应 |
C.该物质1mol能与3 mol氢气发生加成 |
D.该物质在酸性条件下水解能生成两种醇 |
在FeO、Fe2O3和CaCO3的混合物中,已知铁元素的质量分数为56%,则CaCO3的质量分数可能是()
| A.10% | B.25% | C.30% | D.40% |
在一定体积pH=1的HCl与HNO3的混合溶液中,逐滴加入c mol·L-1的AgNO3溶液,当溶液中的Cl-恰好完全沉淀时,溶液pH=2。若反应后溶液的体积等于反应前两溶液体积之和,则原溶液中NO3-的物质的量浓度是()
| A.0.1c mol·L-1 | B.9c mol·L-1 |
| C.(0.1-9c) mol·L-1 | D.(0.9-c)mol·L-1 |
下列各组分子中,范德华力和氢键都存在的是()
| A.苯和CCl4 | B.干冰 | C.HI气体 | D.甲醇和水 |