某实验小组同学为了探究铜与浓硫酸的反应,进行如下实验。
实验1:铜与浓硫酸反应,实验装置如图所示。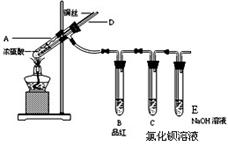
实验步骤:
①先连接好装置,检验气密性,加入试剂;
②加热A试管直到B中品红褪色,熄灭酒精灯;
③将Cu丝上提离开液面;
(1)能够证明铜与浓硫酸反应产生的气体的现象: 。
(2)在盛有氯化钡溶液的C试管中除了导管口有气泡外,无其他明显现象,若将其分为两份,分别滴加下列溶液,将产生沉淀的化学式填入下表相应位置。
| 滴加的溶液 |
氯水 |
氨水 |
| 沉淀的化学式 |
__________________________ |
__________________________ |
写出其中SO2显示还原性的离子方程式: 。
(3)熄灭酒精灯后,因为有导管D的存在,B中的液体不会倒吸,其原因是: 。
(4)将SO2气体通入含有n mol Na2S溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体 mol。 (不考虑溶解的SO2)。
(10分)A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。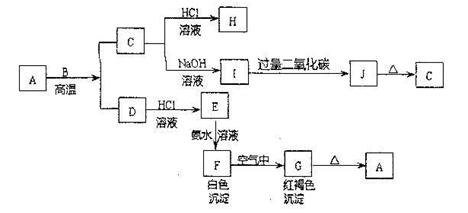
(1)写出下列物质的化学式:
AJ
(2)按要求写方程式:
①C转化为I的离子方程式:。
②F在空气中转化为G的化学方程式:。
③D可以与水蒸气在高温条件下反应,写出此反应的化学方程式:。
Ⅰ.(1)0.02 mol·L-1的HCN溶液与0.02 mol·L-1 NaCN溶液等体积混合,已知该混合溶液中c (Na+)> c(CN-),用“>、<、=”符号填空
①溶液中c(OH -)c(H +) ② c(HCN)c(CN-)
(2)常温下,向Al2(SO4)3溶液中滴入Ba(OH)2溶液至Al3+ 刚好完全沉淀时,溶液pH7,(填“>、<、=”)反应的离子方程式为_____________________________。
Ⅱ.依据氧化还原反应:MnO4-+5Fe2++8H+ = Mn2++5Fe3++4H2O,欲采用滴定的方法测定FeSO4的质量分数,实验步骤如下:
①称量FeSO4样品,配成100 mL待测溶液;
②取一定体积待测液置于锥形瓶中,并加入一定量的硫酸;
③将标准浓度的KMnO4溶液装入滴定管中,调节液面至a mL处;
④滴定待测液至滴定终点时,滴定管的液面读数b mL;
⑤重复滴定2~3次。
(1)如何知道滴定到达终点?_
下列操作会导致测定结果偏低的是___________
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(2)下列每种量器的数量不限,在上述实验中,必须使用的有;
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管
A、B、C三种元素的原子具有相同的电子层数,而B的核电荷数比A大2,C原子的电子总数比B原子电子总数多4。1molA单质跟盐酸反应可置换出11.2L(标准状况下)氢气,这时A转变成与氖原子具有相同电子层结构的离子。试回答:
(1)A_________ B _________ C _________(填化学符号)
(2)分别写出A、B最高价氧化物对应水化物分别跟C的气态氢化物水溶液反应的离子方程式:________________________ ___________________________
(3)A离子的氧化性比B离子的氧化性_______(填“强”或“弱”),这是由于_____________.
已知:下列两个热化学方程式:
Fe(s) + 1/2O2(g)  FeO(s)
FeO(s)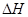 =-272.0KJ/mol
=-272.0KJ/mol
2Al(s) + 3/2O2(g)  Al2O3(s)
Al2O3(s) 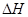 =-1675.7KJ/mol
=-1675.7KJ/mol
则 Al(s)的单质和FeO(s)反应的热化学方程式是______________________________________________________ 。
下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体,化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;反应①是化工生产中的一种重要固氮反应。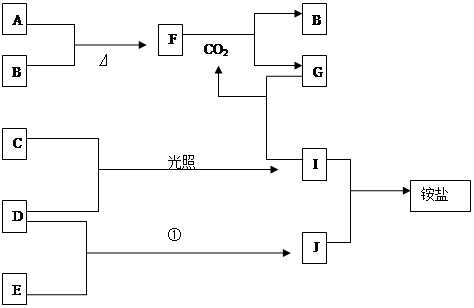
请回答下列问题:
(1)写出下列物质化学式:ABC
(2)写出下列物质间反应的化学方程式
A+B
F+CO2
D+E
I+J
(3)写出下列反应的离子方程式
G+I