最近有研究人员发现了一种处理高浓度乙醛废水的新方法—隔膜电解法,乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸。实验室以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如右图所示。下列说法不正确的是 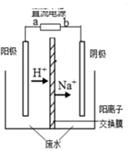
| A.若以CH4—空气燃料电池为直流电源,燃料电池的a极应通入空气 |
| B.阳极反应CH3CHO -2e- + H2O = CH3COOH +2H+ |
| C.电解过程中,阴极区Na2SO4的物质的量增大 |
| D.电解过程中,两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2 |
下列有关能量转化的说法中正确的是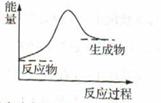
| A.铝热反应属于吸热反应 |
| B.“H—Cl→H+C1"过程中放出热量 |
| C.干冰升华过程放出热量 |
D.反应“C+H2O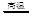 CO+H2” 中的能量变化可以用上图表示 CO+H2” 中的能量变化可以用上图表示 |
将0.1 mol N2和0.3 mol H2置于密闭容器中发生反应:N2+3H2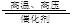 2NH3,下列关于该反应的说法中正确的是
2NH3,下列关于该反应的说法中正确的是
| A.增大压强,反应速率减小 |
| B.最终可生成0.2 mol NH3 |
| C.升髙温度,反应速率增大 |
| D.当V正(N2):V 正(H2)=1:3时,一定达化学平衡状态 |
己知向NaNO2溶液中加入酸性KMn04溶液发生如下反应:
2KMn04+5NaN02+3H2S04=2MnS04+5NaN03+K2S04+3H20有关该反应的下列说法中正确的是
| A.KMn04作氧化剂 | B.该反应不属于离子反应 |
| C.氮元素被还原 | D.当反应中转移10 mol电子时,生成lmol MnS04 |
下列装置所示的实验,能达到实验目的的是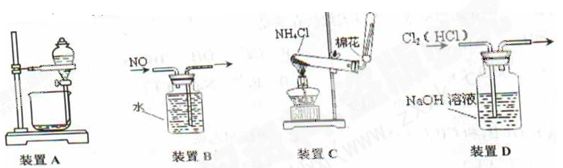
| A.用装置A分离乙酸和乙酸乙酯 | B.用装置B收集NO气体 |
| C.用装罝C在实验室中制取氨气 | D.用装置D除去Cl2中的HC1 |
下列反应的离子方程式正确的是
| A.氢氧化铜与盐酸反应:H++OH- =H2O |
| B.铝与氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑ |
| C.铁与稀硝酸反应 Fe +2 H+= Fe2++H2↑ |
| D.硫酸铜与氢氧化钡洛液反应Cu2++S042-+Ba2++20H =Cu(0H)2↓ +BaS04 ↓ |