单斜硫和正交硫转化为二氧化硫的能量变化如图所示,下列说法正确的是 ( )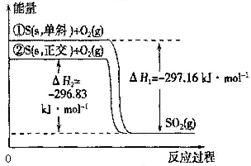
| A.S(s,单斜) = S(s,正交) △H =" +" 0.33 kJ·mol-1 |
| B.相同物质的量的正交硫比单斜硫所含有的能量高 |
| C.正交硫比单斜硫稳定 |
| D.①表示断裂1mol O2中的共价键所吸收的能量比形成l mol SO2中的共价键所放出的能量少297.16 kJ |
以下说法不正确的是 ( )
| A.浊液的分散质粒子直径大于100nm ,不能通过滤纸 。 |
| B.溶液的分散质粒子直径小于1nm,能通过滤纸 。 |
| C.胶体的分散质粒子直径小于100nm但大于1nm,能通过滤纸 。 |
| D.胶体的分散质粒子直径小于100nm但大于10nm,不能通过滤纸。 |
在反 应X + 2Y =" R" + 2M中,已知R和M的摩尔质量之比为22 : 9,当1.6g的X与Y完全反应后,生成4.4g的R。则在此反应中Y和M的质量之比为
应X + 2Y =" R" + 2M中,已知R和M的摩尔质量之比为22 : 9,当1.6g的X与Y完全反应后,生成4.4g的R。则在此反应中Y和M的质量之比为
| A.16 : 9 | B.23 : 9 | C.32 : 9 | D.46 : 9 |
对于某些离子的检验及结论一定正确的是
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32‒ |
B.加入氯化钡 溶液有 溶液有 白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42‒ 白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42‒ |
| C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③ 13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是:
13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表达正确的是:
a.体积 ②>③>①>④ b.密度 ②>③>④>①
c.质量 ②>③>①>④ d.氢原子个数 ①>③>④>②
| A.abc | B.bcd | C.abcd | D.acd |
分别将等物质的量浓度的KCl、MgCl2、AlCl3三种溶液中的Cl‒完全沉淀,消耗相同物质的量浓度的AgNO3溶液的体积比为3 : 2 : 1,则上述三种溶液的体积比为
| A.1:1:1 | B.6:3:2 | C.3:2:1 | D.9:3:1 |