已知:HCN(aq)+ NaOH(aq) ==NaCN(aq)+H2O(l) ΔH=-12.1 kJ·mol-1;
HCl(aq)+NaOH(aq) ==NaCl (aq)+H2O(l) ΔH=-55.6 kJ·mol-1
则HCN在水溶液中电离的ΔH等于
| A.+43.5 kJ·mol-1 | B.+67.7 kJ·mol-1 |
| C.-43.5 kJ·mol-1 | D.-67.7 kJ·mol-1 |
白磷在高压下隔绝空气加热后急速冷却,可得钢灰色固体——黑磷,其转化过程如下:
白磷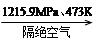 黑磷,黑磷比白磷稳定,结构与石墨相似。下列叙述正确的是
黑磷,黑磷比白磷稳定,结构与石墨相似。下列叙述正确的是
| A.白磷转化为黑磷是吸热反应 | B.黑磷与白磷互为同分异构体 |
| C.白磷转化为黑磷是氧化还原反应 | D.黑磷能导电 |
下列相关反应的离子方程式书写正确的是
| A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B.硫酸铜溶液显酸性:Cu2+ + 2H2O=Cu(OH)2↓+ 2H+ |
| C.向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH- =NH3↑+H2O |
| D.用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
某有机物A的分子式为C4H8Cl2,分子中只有一个甲基,则A的结构有
| A.2种 | B.3种 | C.4种 | D.5种 |
下列对有机物结构或性质的描述,错误的是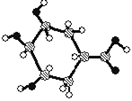
| A.某有机物球棍结构模型如上图,则该有机物能发生消去反应和氧化反应 |
| B.光照下2,2—二甲基丙烷与Br2蒸气反应,其一溴取代物只有一种 |
| C.乙烷和丙烯的物质的量共1 mol,完全燃烧生成3 mol H2O |
| D.二十碳五烯酸和二十二碳六烯酸是鱼油的主要成分,它们含有相同的官能团,是同系物,化学性质相似 |
生活中下列处理方法正确的是
| A.蚂蚁叮咬的红肿处涂沫苯酚止痒 | B.冬天在汽车水箱中加乙二醇抗冻 |
| C.纺织品上的油腻用烧碱溶液清洗 | D.把铁器具浸入水隔绝空气防生锈 |