下离子方程式H++OH-=H2O所表示的反应是( )
| A.所有酸和碱之间的中和反应 |
| B.所有强酸和强碱之间的中和反应 |
| C.所有可溶性酸和可溶性碱之间的中和反应 |
| D.强酸溶液与强碱溶液生成可溶性盐和水的反应 |
关于容量瓶的使用,下列操作正确的是
| A.使用前要检验容量瓶是否漏液 |
| B.用蒸馏水荡洗后必须要将容量瓶烘干 |
| C.为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行 |
| D.为了使所配溶液浓度均匀,定容结束后,手握瓶颈,左右振荡 |
下列物质中,能够导电的电解质是
| A.Cu丝 | B.熔融的MgCl2 |
| C.NaCl溶液 | D.蔗糖 |
氧化还原反应的实质是
| A.氧元素的得与失 | B.化合价的升降 |
| C.电子的得失或偏移 | D.分子中原子重新组合 |
25℃,有c(CH3COOH)+c(CH3COO-)=0.1mol·L-1的一组醋酸和醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示。下列有关离子浓度关系叙述正确的是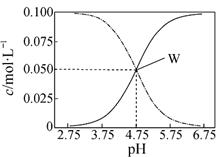
| A.pH=5.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
| B.W点表示溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) |
| C.pH=3.5溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1mol·L-1 |
| D.向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化可忽略): |
c(H+)=c(CH3COOH)+c(OH-)
一定条件下,溶液的酸碱性对TiO2光催化燃料R降解反应的影响如下图所示。下列判断判断正确的是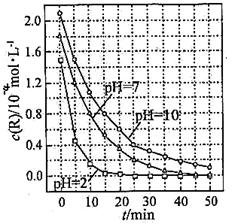
| A.在0−50min之间,pH=2和pH=7时R的降解百分率相等 |
| B.溶液酸性越强,R的降解速率越小 |
| C.R的起始浓度越小,降解速率越大 |
| D.在20−25min之间,pH=10时R的平均降解速率为0.04 mol·L-1·min-1 |