下列离子方程式正确的是
| A.向澄清石灰水中加入等物质的量的NaHCO3溶液:Ca2++2OH-+ 2HCO3- = CaCO3↓+CO32-+2H2O |
| B.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全: Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4↓+ NH3·H2O + H2O |
| C.氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
| D.明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值: |
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
将两粒相同大小的钠,一粒用铝箔包好为甲,另一粒为乙,将甲、乙两粒钠分别投入足量的水中,收集所得气体,气体的体积大小关系是()
| A.甲多 | B.乙多 | C.一样多 | D.无法确定 |
一未完成的离子方程式:________+XO+6H+===3X2+3H2O,据此判断下列说法
正确的是()
| A.X原子最外层有5个电子 |
| B.当有1molX2生成时,共有2mol电子转移 |
| C.氧化产物和还原产物的物质的量之比为5∶1 |
| D.“_____”上所填的微粒和XO在任何环境下都不能共存 |
下列物质的制备方法正确的是()
| A.氯化铝溶液和硫化钠溶液反应制备Al2S3 |
| B.用镁粉和空气反应制备Mg3N2 |
| C.用铝粉和MnO2制得锰 |
| D.用电解熔融氯化铝的方法制得单质铝 |
下列离子方程式书写正确的是()
| A.过量的CO2通入NaOH溶液中:CO2+2OH-= CO32-+H2O |
| B.氨水中通入过量CO2:2NH3·H2O + CO2 = 2NH4+ + CO32— + H2O |
| C.饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液:Ca2++HCO3—+OH—=CaCO3↓+H2O |
| D.NaHCO3溶液中加入过量的Ca(OH)2溶液:2HCO3- +Ca2++2OH-= CaCO3↓+2H2O+CO32- |
室温下,下列各组离子能大量共存的是()
| A.稀硫酸中:K+、Mg2+、AlO2-、S2O32- |
| B.Na2S溶液中:SO42-、K+、Cl-、Cu2+ |
C.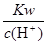 =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42- =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42- |
| D.通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- |