某纯碱样品中含有少量氯化钠杂质,为了测定此样品纯度,甲同学设计了下图所示装置和实验方案。实验步骤如下: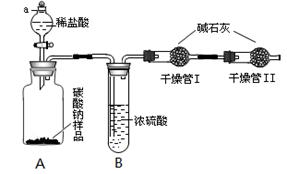
①按图将仪器组装好并检查气密性;
②准确称量盛有碱石灰的干燥管Ⅰ的质量(设为m1);
③准确称量纯碱样品的质量(设为n),放入广口瓶A内;
④打开分液漏斗a的旋塞,缓缓滴入稀盐酸,至不再产生气泡为止;
⑤称量干燥管Ⅰ的质量(设为m2)。
(1)实验操作④要缓缓地进行,其理由是_________。如果操作太快,会导致测定结果________(填偏大、偏小或不变)。
(2)装置B的作用是_____________________;干燥管Ⅱ的作用是___________________。
(3)根据甲同学的实验数据,写出计算纯碱样品纯度的公式_______________________。
(4)方案评价:乙同学认为甲同学的方案有缺陷。乙同学认为稀盐酸要改为稀硫酸,否则会导致测定结果偏大。你认为还有其它缺陷吗?如果有,提出你的改进意见或需要添加的实验步骤,并指出甲同学缺少这一步骤会对结果产生什么影响(填偏大、偏小或不变),将答案填入表中(不一定要填满)。
| 序号 |
改进意见 |
缺少时的影响 |
| ① |
|
|
| ② |
|
|
| ③ |
|
|
有人设计了如右图所示实验装置,目的是做钠与水反应的实验并验证:
①钠的物理性质②钠与水反应的产物是什么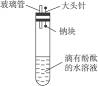
(1)当进行适当操作时还需要的仪器有_________________________________。
(2)如何进行操作?____________________________________。
(3)实验现象是________________________________________。
在课堂上,老师演示了金属钠与CuSO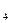 溶液的反应,同学们观察到该反应中生成了蓝色的Cu(OH)
溶液的反应,同学们观察到该反应中生成了蓝色的Cu(OH)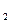 沉淀而没有发现铜单质生成。但某同学想:会不会因生成的铜较少被蓝色沉淀所覆盖,而没有被发现呢?于是他想课后到实验室继续研究,希望进一步用实验来验证自己的猜测是否正确。
沉淀而没有发现铜单质生成。但某同学想:会不会因生成的铜较少被蓝色沉淀所覆盖,而没有被发现呢?于是他想课后到实验室继续研究,希望进一步用实验来验证自己的猜测是否正确。
假如该同学是你,请你写一张实验准备单交给老师,要求老师提供必需的用品。
(1)实验探究目的:___________________________。
(2)探究所依据的化学原理:____________________________。
(3)实验必需仪器:小刀、玻璃片、滤纸、_________和__________;药品:金属钠、_____和___________。该同学在探究实验中意外地发现生成的蓝色沉淀中混有少量的黑色难溶物,而所使用的药品均没有问题,你认为该黑色难溶物是___________,生成该黑色难溶物的原因是_______________________________________________。
某课外小组在做过氧化钠与水反应的实验时,发现向反应后的溶液中滴加酚酞试液时,溶液呈现红色,但红色很快褪去。根据对实验现象的观察和思考,甲、乙、丙3位同学分别提出了自己的推测。
甲:反应时试管很热,可能是溶液温度较高使红色褪去。
乙:由于所加水较少,可能是氢氧化钠溶液浓度较大使红色褪去。
丙:过氧化钠会跟有色物质结合成不稳定的无色物质,从而使红色褪去。
(1)验证甲同学的推测是否正确的方法是:_______________________________________。
(2)验证乙同学的推测是否正确的方法是:_______________________________________。
(3)验证丙同学的推测是否正确的方法是:_______________________________________。
在呼吸面具和潜水艇中可用过氧化钠作为供氧剂,请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可作供氧剂。
(1)A是制取CO2的装置,写出A中发生反应的化学方程式:_________________________。
(2)填写表中空格:
| 仪器 |
加入试剂 |
加入该试剂的目的 |
| B |
饱和碳酸氢钠溶液 |
|
| C |
||
| D |
(3)写出过氧化钠与二氧化碳反应的化学方程式:________________________________。
(4)试管F中收集满气体后,下一步实验操作是__________________________________。
给你提供40 g NaOH固体、足量的蒸馏水和足量的CO2气体,你怎样把NaOH完全转化成Na2CO3?