(1)已知在K2Cr2O7的溶液中存在如下平衡: Cr2O72-(橙色)+H2O 2CrO42-(黄色)+2H+,向5mL0.1mol/L K2Cr2O7溶液中滴加3-10滴浓H2SO4,观察到的现象为__________;在此基础上再滴加5-10滴6mol/LNaOH溶液,溶液颜色变化为__________。
2CrO42-(黄色)+2H+,向5mL0.1mol/L K2Cr2O7溶液中滴加3-10滴浓H2SO4,观察到的现象为__________;在此基础上再滴加5-10滴6mol/LNaOH溶液,溶液颜色变化为__________。
(2)已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列叙述正确的是__________(填序号)。
①生成物的产量一定增加
②生成物的体积分数一定增加
③反应物的浓度一定降低
④反应物的转化率一定增加
⑤正反应速率一定大于逆反应速率
有机物A的结构简式为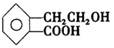 ,它可通过不同化学反应分别制得B、C、D 和E四种物质。
,它可通过不同化学反应分别制得B、C、D 和E四种物质。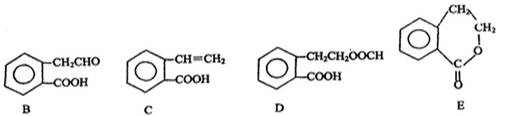
请回答下列问题:
(1)指出反应的类型:A→B,A→C。
(2)写出物质B。
(3)在A~E五种物质中,互为同分异构体的是(填代号)。
(4)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是(填序号)。
(5)C能形成高聚物,该高聚物的结构简式为。
(6)写出由A生成E的化学方程式:。
按要求完成下列问题:
(1)N2(g)和H2(g)反应生成1molNH3(g)放出46.1KJ热量。
(2)航天领域使用氢氧燃烧电池有酸式和碱式两种,它们放电时的总反应可以表示为:2H2 + O2 =2H2O,酸式氢氧燃烧电池的电解池是酸。其负极反应可以表示为2H2-4e-=4H+,则其正极反应可以表示为;;碱式氢氧燃烧电池的电解质是碱,其正极反应可以表示为:O2+2H2O+4e-=4OH-,则其负极反应可以表示为:。
(3)用石墨作电极电解NaCl水溶液,阴极的电极反应。
(4)在粗铜精炼的反应中,当阳极,阳极的电极反应。
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置。
(1)把化学能转化为电能的装置是(填“甲”或“乙”);
(2)甲中②的电极名称为。
(3)④电极上的电极反应式为。
(4)①电极上的电极反应式为 ,
检验该电极反应产物的方法是。
(5)写出装置甲的反应总化学方程式。
2SO2(g)+ O2(g) 2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1molSO3(g)的ΔH =" -99" kJ·mol-1
2SO3(g)反应过程的能量变化如图所示。已知1mol SO2(g)氧化为1molSO3(g)的ΔH =" -99" kJ·mol-1
请回答下列问题:
(1)图中A表示。该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?加入V2O5后,上述反应ΔH(填变大、不变、变小)
(2)图中ΔH = kJ·mol-1。
(3)如果反应速率v(SO2)为0.06 mol·L-1·min-1,则v(O2)为mol·L-1·min-1。
(4)已知S(s) + O2(g) = SO2(g) ΔH =" -296" kJ·mol-1,则由S(s)生成5 mol SO3(g)的ΔH=kJ·mol-1。
(1)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)===2CO(g)ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:____________________。
(2)在25℃,101KPa时,CO的燃烧热为280kJ/mol,写出 CO的燃烧热的热化学方程式:____________________________。
(3)在火箭推进器中以肼(N2H4)作为燃料,可以选O2或NO2作为氧化剂,如果以氧气作为氧化剂,其化学反应与能量关系如下,
请写出该反应的热化学方程式 :_______________________________________。