(9分)某100mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0.4mol/L。现将一定量的铁粉投入到该溶液中,回答下列问题:
(1) CuCl2的电离方程式为 , 铁粉投入后反应的离子方程式为 。
(2)原溶液中Cu2+的浓度为 mol/L。
(3)反应后测得Cl-的浓度为 mol/L。
(4)若反应后测得Fe2+的溶液为0.1mol/L,则反应生成铜单质的质量为 g。剩余的Cu2+的浓度为 mol/L。
由于Fe(OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱溶液反应制得Fe(OH)2白色沉淀。若用下图所示实验装置,则可制得纯净的Fe(OH)2白色沉淀。已知两极材料分别为石墨和铁: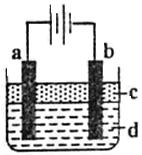
(1)a极材料为,a电极反应式为。
(2)电解液d可以是,则白色沉淀在电极上生成;电解液d也可以是,则白色沉淀在两极间的溶液中生成。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
(3)液体c为苯,其作用是,在加苯之前对d溶液进行加热煮沸处理,目的是。
(4)为了在短时间内看到白色沉淀,可以采取的措施是。
A.改用H2SO4作电解液 B.适当增大电源电压
C.适当缩小两极间距离 D.适当地降低电解液的温度
(5)若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源继续电解,除了电极
上看到的气泡外,另一明显的现象为。
(12分) 电化学原理在化学工业中有广泛应用。请根据下图回答有关问题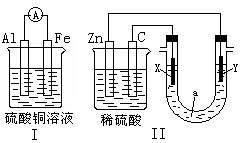
(1)装置I中能量的转化形式是。导线上电子定向移动方向从极到极。其电极反应式。
(2)装置II中若X、Y都是惰性电极,a是CuCl2溶液。则发生氧化反应的电极是和。检验X电极反应产物的方法是。
若a是饱和NaCl溶液(氯碱工业生产原理),电极材料是石墨电极和铁电极。实验开始时,同时在两极各滴入几滴酚酞试液,则(填“石墨或铁”)附近溶液先变红,其电极反应式。
(3)当装置I和装置II的电路中均转移0.2mol电子时,则装置I中铁电极质量的变化
g(填写“增加”或“减少”及具体质量),装置II中收集到的气体共有L(标准状况下)(以装置II中X、Y是惰性电极,a是CuCl2溶液计算)。
(8分) 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
2SO2(g)+O2(g)  2SO3(g) △H=-190 kJ·mo1-1
2SO3(g) △H=-190 kJ·mo1-1
(1)在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(O2)=______mol·L-1·min-1
(2)下列条件的改变对其反应速率几乎无影响的是(选填序号)
①升高温度 ②保持体积不变,只增加氧气的质量 ③保持体积不变,充入Ne使体系压强增大 ④保持压强不变,充入Ne使容器的体积增大
(3)下列描述中能说明上述(1)反应已达平衡的是(选填序号)
①v(O2)正=2v(SO3)逆 ②SO2、O2、SO3的浓度之比为2:1:2
③单位时间内生成2n molSO2的同时生成2n mol SO3
④容器中气体的平均分子量不随时间而变化
⑤容器中气体的密度不随时间而变化 ⑥容器中气体压强不随时间而变化
(4)在相同条件下发生上述反应,若要得到380kJ热量,则加入各物质的物质的量可能是。
| A.4 mo1SO2和2mol O2 | B.4mol SO2、2mo1 O2和2mol SO3 |
C.4mol SO2和4 mo1 O2 | D.6mo1 SO2和4 mo1 O2 |
(12分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题: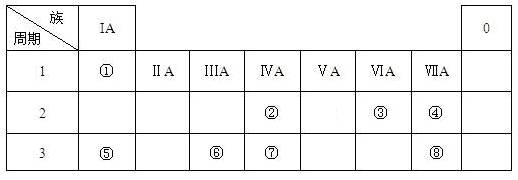
(1)④、⑤、⑥的原子半径由大到小的顺序为_______________________,②、⑦、⑧的最高价含氧酸的酸性由强到弱的顺序是______________________。
(2)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)_________________。
a.MnO2 b.FeCl 3 c.Na2SO3 d.KMnO4
若已知1 克该液态化合物分解成③的单质和一种常见液体时,可放出2.89kJ能量,写出该反应的热化学方程式:
(3)工业上常采用电解A和冰晶石(Na3AlF6)混合物的方法冶炼制备⑥的单质,请从A晶体的类型和微粒间的相互作用力角度解释加冰晶石(Na3AlF6)的原因。并写出电解时的电极反应式:。
(4)甲、乙、丙是上述部分元素组成的双原子分子或负二价双原子阴离子,且甲、乙、丙的电子总数相等。甲是一种极强的氧化性单质。丙与⑤的阳离子可形成一种淡黄色固体B,该固体跟水反应可得到③的单质。则B中化学键的类型,乙的电子式,甲的组成元素的原子结构示意图,能证明甲的组成元素非金属性很强的事实。(任举一例即可)
现有①BaCl2②金刚石③金属铜④KOH ⑤干冰⑥纯硫酸⑦二氧化硅⑧白磷⑨K2O⑩NH4Cl十种物质,按下列要求回答(填序号):
⑴熔化时需要破坏共价键的是;⑵属于分子晶体的是;
⑶固体不导电,常压下熔化时能导电的是;⑷④的电子式。