将不同量的H2O(气) 和CO 气体分别通入到一体积为l L的恒容密闭容器中进行反应:H2O (g) + CO( g) 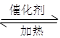 CO2 (g) +H2(g);得到以下三组数据,据此回答下列问题:
CO2 (g) +H2(g);得到以下三组数据,据此回答下列问题:
| 实验组 |
温度 |
起始量 |
平衡量 |
达到平衡所需时间 |
||
| H2O |
CO |
H2 |
CO |
|||
| 1 |
650℃ |
1 mol |
2 mol |
0.8 mol |
1.2 mol |
5 min |
| 2 |
900℃ |
0.5 mol |
1 mol |
0.2 mol |
0.8 mol |
3 min |
| 3 |
900℃ |
a |
b |
c |
d |
t |
(1)①由以上数据,实验1中以v( CO2) 表示的反应速率为__________。
②该反应在650℃时平衡常数数值为__________,该反应的逆反应为__________ (填“吸” 或“放”)热反应。
③若实验3要达到与实验2相同的平衡状态(即各物质的质量分数分别相等),且t <3min,则a、b 应满足的关系是__________。
(2)下图1、2 表示上述反应在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化的情况:
①图1中时刻t2发生改变的条件可能是__________ (写2条)
②图2中时刻t2发生改变的条件可能是__________ (写2条)
(3)在850℃时,其平衡常数K = 1,850℃时在该容器中同时充人1.0moICO,3.0 molH2O,1.0molCO2,5.0molH2,此时反应向__________(填“正反应” 或“逆反应”)方向进行,平衡时CO2的物质的量为__________。
有机物A(C6H8O4)为食品包装纸的常用防腐剂。A可以使溴水褪色。A难溶于水,但在酸性条件下可发生水解反应,得到B(C4H4O4)和甲醇。通常状况下B为无色晶体,能与氢氧化钠溶液发生反应。
(1)A可以发生的反应有___________________(选填序号)。
①加成反应②酯化反应③加聚反应④氧化反应
(2)B分子所含官能团的名称是_____________、_____________。
(3)B分子中没有支链,其结构简式是__________________________,B的具有相同官能团的同分异构体的结构简式是__________________________。
(4)由B制取A的化学方程式是________________________________________________。
(5)天门冬氨酸(C4H7NO4)是组成人体蛋白质的氨基酸之一,可由B通过以下反应制取:
B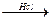 C
C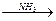 天门冬氨酸
天门冬氨酸
天门冬氨酸的结构简式是________________________。
下面是一个合成反应的流程图。A—G均为有机物,反应中产生的无机物均省略,第一步反应中的试剂与条件有的已注明、有的未注明。根据图填空: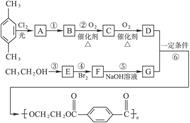
(1)写出D的分子式____________________,G的结构简式________________。
(2)写出下列化学反应方程式并注明反应类型
反应②___________________________,____________。
反应⑤___________________________,____________。
反应⑥___________________________,____________。
(3)写出两种符合括号内条件的D的同分异构体的结构简式(苯环上有两个取代基,在对位且属于酯类):
_____________________________、_____________________________。
(4)试计算该流程中,每生产1.00吨高分子化合物,理论上消耗NaOH固体_______吨。
(5)绿色化学追求充分利用原料中原子,实现零排放或少排放。就该流程中大量消耗NaOH,谈一谈你的建议或设想:
______________________________________________________________________________。
(9分)葡萄糖是人类的营养素。在人体里。富氧条件下氧化生成CO2和H2O;在缺氧条件时,则生成一种有机酸A。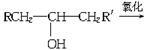
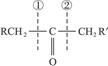

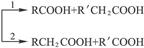
已知:将A进行如下图所示的反应。其中C和C′是同系物。C′是甲酸(HCOOH)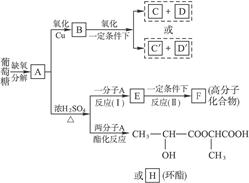
完成下列问题:
(1)C和D′属于_________(用编号填入,以下同)。
①同系物②同分异构体③同类物质④同素异形体
(2)D′与E分别属于哪一类化合物:D′_________,E_________。
①多元醇②醛③不饱和羧酸④多元羧酸⑤酯
(3)写出结构简式:A_________,F_________,H_________。
(4)写出反应类型:Ⅰ__________,Ⅱ__________。
(5)写出A→E的化学反应方程式:_____________________________。
已知: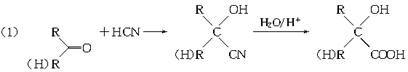
(2)R—CHCH2+HBr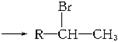
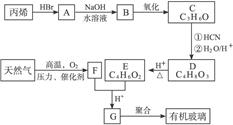
有机玻璃可按下列路线合成:
F亦可由水煤气在高温、高压、催化剂存在下合成。试写出:
(1)天然气的主要成分和C的结构简式分别为_________、_________。
(2)E+F G的反应方程式为______________________________________。
G的反应方程式为______________________________________。
(3)丙烯 A和A
A和A B的反应类型分别属于___________、___________。
B的反应类型分别属于___________、___________。
(4)G 有机玻璃的反应方程式为__________________。
有机玻璃的反应方程式为__________________。
某多肽在小肠液的作用下完全水解得到甘氨酸 (相对分子质量为75)、丙氨酸
(相对分子质量为75)、丙氨酸 (相对分子质量为89)、半胱氨酸
(相对分子质量为89)、半胱氨酸 (相对分子质量为121)三种氨基酸。现称取该多肽830 g,完全水解后共得到1010 g氨基酸,经分析该氨基酸混合物的平均相对分子质量为100,1 mol多肽含硫原子50 mol。问:
(相对分子质量为121)三种氨基酸。现称取该多肽830 g,完全水解后共得到1010 g氨基酸,经分析该氨基酸混合物的平均相对分子质量为100,1 mol多肽含硫原子50 mol。问:
(1)若使上述氨基酸中的氮全部转化为铵盐,并加碱中和,全部蒸出氨气,可得氨气_____
________g。
(2)一分子此多肽完全水解生成________个氨基酸。