用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: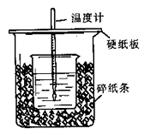
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
(16分)孔雀石的主要成分为Cu2(OH)2CO3,还含少量铁的氧化物和硅的氧化物。以下是实验室以孔雀石为原料制备CuSO4·5H2O晶体的流程图:
(1)孔雀石研磨的目的是。浸泡孔雀石的试剂A若选用过量的稀硫酸,则产生的气体a是(填化学式)、固体a是(填化学式)。
(2)使用试剂B的目的是将溶液中的Fe2+转化为Fe3+,试剂B宜选用(填选项序号)。
A.酸性KMnO4溶液 B.双氧水 C.浓硝酸 D.氯水
相应的化学反应方程式:。
(3)试剂C的使用目的是调节溶液pH,使Fe3+转化为沉淀予以分离。试剂C宜选用(填选项序号)。
A.稀硫酸 B.NaOH溶液 C.氨水 D.CuO
相应的离子方程式。
(4)1 mol氨气通过加热的Cu2(OH)2 CO3可以产生1.5 mol金属铜,发生反应的化学方程
式:。
(5)常温下Fe(OH)3的Ksp=1×10-39,若要将溶液中的Fe3+转化为Fe(OH)3沉淀,使溶液中c(Fe3+)降低至1×10—3 mol/L,必需将溶液pH调节至。
(14分)下图所示是用于气体制备、干燥(或除杂质)、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去,各装置可重复使用也可不用)。请根据下列要求回答问题。
(1)若用A-C-D-B组合进行氢气还原氧化铜实验。分液漏斗中的试剂是盐酸,C中试剂是水,其作用是;A中反应开始后,加热B之前的实验操作是,加热后B中将观察到的现象是。B中反应的化学方程式。
(2)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系。A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是;C中试剂是,D的作用是。
(3)为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na2O2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是(填字母);装置B中可能发生反应的化学方程式为:。
实验室制取并收集氯气的装置如右图:某同学进行实验时可能有如下操作: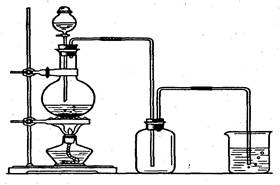
(1)烧瓶中发生反应的化学方程式是:___________________________。
(2)制得的氯气可选用____________来干燥,烧杯中发生反应的离子方程式是_________________。
(3)在实验室里,常用加热食盐晶体和浓硫酸的混合物的方法来制取HCl,HCl是一种无色有刺激性气味的气体,密度比空气大,极易溶于水,它的水溶液叫氢氯酸,即盐酸。
①实验室制取HCl的发生装置可选用制_____的发生装置(填O2、Cl2、CO2中的一种)。
②收集氯化氢气体时应采用__________法。
③实验室可用__________________________试纸放在瓶口检验HCl是否充满了集气瓶。
④上图哪些装置可作为多余氯化氢的吸收装置?______________________________。
(共9分)已知NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,某混合物A含有
KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化: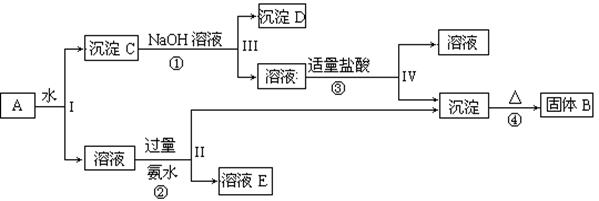 据此回答下列问题:
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是。
(2)根据上述框图反应关系,写出下列B、D所含物质的化学式
固体B;沉淀D;
(3)写出①、②、④四个反应的化学方程式,是离子反应的写出离子方程式
①;
②;
④ 。
。
(共12分)在容积固定为2L的密闭容器中,充入0.180 molHI,480℃时反应:
2HI(g) H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
H2(g)+I2(g),体系中n(HI)随时间变化情况如下表:
| t/min |
0 |
2 |
4 |
6 |
8 |
10 |
| n(HI)/mol |
0.180 |
0.164 |
0.152 |
0.144 |
0.140 |
0.140 |
反应进行至10min后将反应混合物的温度降低,发现气体的颜色变浅。
(1)0~2min内H2的平均反应速度为。达平衡时,HI的转化率是_________。(2)上述正向反应是:反应(选填:放热、吸热)。
(3)某温度下上述反应平衡时,恒容、升高温度,原化学平衡向反应方向移动(填“正”或“逆”),正反应速率(填“增大”、“减小”或“不变”),容器内混合气体的压强(填“增大”、“减小”或“不变”)。
(4)480℃时,反应H2(g)+I2(g) 2HI(g)的平衡常数K的值为。
2HI(g)的平衡常数K的值为。
(5)要增大反应2HI(g) H2(g)+I2(g)的平衡常数,可采取的措施是(选填字母)。
H2(g)+I2(g)的平衡常数,可采取的措施是(选填字母)。
A.增大HI起始浓度
B.向混合气体中通入I2
C.使用高效催化剂
D.升高温度