下图所示是分离混合物时常用的仪器,回答下列问题:
(1)写出仪器C、E的名称 、
(2)分离以下混合物应该主要选用上述什么仪器?(填字母符号)
①NaCl固体和泥沙: ②花生油和水:
(3)若向C装置中加入碘水和足量CCl4,充分振荡后静置,观察到现象是:C内液体分两层,上层液体 色,下层液体 色。
(4)碘单质和溴单质有相类似的性质,都可以用有机溶剂萃取水溶液中的单质,若利用C仪器提取溴水中的溴单质,下列有机溶剂中不能选用的是:
A.汽油 B.CCl4 C.酒精 D.醋酸
已知氯水中有如下平衡:Cl2+H2O HCl+HClO。常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸人40mLCl2和10mL H2O。
HCl+HClO。常温下在一个容积为50mL的针筒(如图所示,活塞可自由滑动,针筒上有刻度)里吸人40mLCl2和10mL H2O。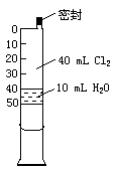
(1)针筒中可观察到的现象是________________。
(2)若将此针筒长时间放置在有日光的地方,最终可能观察到的现象是________________。
(3)用化学平衡的观点解释(2)的现象:________________。
试设计一套实验方案验证某白色粉末是纯碱。
某校化学研究性学习小组利用下面所提供的仪器装置和药品制取NaHCO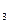 溶液,设计如下实验。实验室提供的药品、仪器装置如下:
溶液,设计如下实验。实验室提供的药品、仪器装置如下:
药品:①2% NaOH溶液②稀HCl③稀H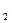 SO
SO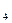 ④饱和KHCO
④饱和KHCO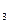 溶液⑤浓H
溶液⑤浓H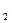 SO
SO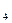 ⑥CaCO
⑥CaCO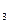 固体⑦K
固体⑦K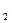 CO
CO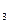 粉末
粉末
仪器装置(如图所示):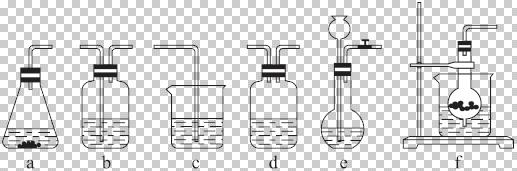
请根据题目要求完成下列问题:
(1)请按下表要求,填写选择的装置和药品。
| 分项 内容 |
CO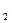 发生装置 发生装置(随开随用,随关随停) (X) |
除杂洗 气装置 (Y) |
制备产 品装置 (Z) |
| 选择的装置 (填序号) |
C |
||
| 选择的药品 (填序号) |
① |
(2)如何检验所选择的CO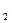 发生装置(X)的气密性,请写出主要操作过程:__________。
发生装置(X)的气密性,请写出主要操作过程:__________。
(3)将装置按X、Y、Z顺序连接并检查气密性后,当加入药品实验时,X装置中发生化学反应的离子方程式为_____________,Y装置中除去的杂质为_________________。
(4)常温下,向Z装置的NaOH溶液中通入过量CO2气体,其目的是______________。
(5)若要保证Z装置中不析出晶体(不考虑过饱和溶液问题),NaOH溶液最大浓度不能超过________________%(质量分数)。
附:有关物质在常温(25 ℃)时的溶解度
| 化学式 |
Na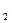 CO CO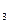 |
NaHCO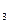 |
NaOH |
NaCl |
Na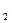 SO SO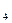 |
| 溶解度 (g/100 g H 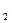 O) O) |
21.3 |
9.60 |
107 |
35.8 |
19.4 |
某天然碱的化学组成可能为aNa2CO3·bNaHCO3·cH2O (a、b、c为正整数),为确定其组成,化学兴趣小组的同学进行了如下实验:
(1)定性分析:
①取少量天然碱样品放入试管中,用酒精灯加热,在试管口有液体生成,该液体能使无水硫酸铜变蓝。能否说明样品中含结晶水,试简述理由。_________________________________。
②请你设计一个简单的实验方案,确认样品中含有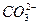 。
。
______________________________________________________________________________。
(2)定量分析:该小组同学设计了下图所示装置,测定天然碱的化学组成。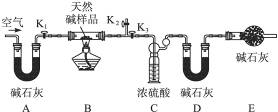
实验步骤:
①按上图(夹持仪器未画出)组装好实验装置后,首先进行的操作是____________________。
A处碱石灰的作用是_______________,E处碱石灰的作用是__________________________。
②称取天然碱样品7.3 g,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶的质量为87.6 g,装碱石灰的U形管D的质量为74.7 g。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热,待不再产生气体为止。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后称得装浓硫酸的洗气瓶质量为88.5 g;装碱石灰的U形管D的质量为75.8 g。该步骤中缓缓鼓入空气数分钟的目的是_____________。计算推导:该天然碱的化学式为_____________。
有人设计了如右图所示的实验装置,目的是做钠与水反应的实验并验证:①钠的物理性质;②钠与水反应的产物是什么。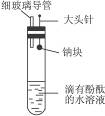
(1)当进行适当操作时还需要的仪器有_________________________________;
(2)如何进行操作?_____________________________________________________________;
(3)实验现象是________________________________________________________________。