按下列要求各举一例,写出有关化学方程式,并标出电子转移的方向和数目。
(1)氢气还原一种非金属单质______________________
(2)同一种物质中的一种元素被氧化,另一种元素被还原________________
(3)同种元素不同物质间的氧化还原反应__________________________
(4)一种固体非金属单质置换另一种气体非金属单质______________________
由短周期元素组成的A、B、C、D、E、F六种微粒,其中只有C、D是分子,其余四种均为带一个单位正电荷的阳离子或一个单位负电荷的阴离子,且每个微粒中都含有10个电子。已知A、E是由非金属元素组成的阳离子,六种微粒间有下列关系:
①A++B-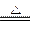 C+D, B-+E+=2
C+D, B-+E+=2 D;
D;
②通常情 况下,C是一种无色刺激性气味的气体,且可使湿润的红色石
况下,C是一种无色刺激性气味的气体,且可使湿润的红色石 蕊试纸变蓝;
蕊试纸变蓝;
③向含F离子的溶液中加入C的水溶液,可生成白色沉淀W,C溶液过量沉淀也不消失。再加入含大量B离子或大量E离子的溶液时,沉淀W在其中一种情况下溶解,另一种情况下不溶解。
请回答下列问题:
(1)微粒A的名称及化学式分别为、。
(2)C的水溶液中存在的分子总数至少有种。
(3)写出微粒F与过量C的水溶液反应的离子方程式:。
(4)向含有0.1mol F离子的50mL溶液中,加入含1.5mol/L B离子的200mL强碱溶液,结果有白色沉淀产生,再向该混合物中加入含1mol/L E离子的强酸溶液,若要使沉淀恰好溶解,则最后加入的溶液的体积至少为mL。
若以X、 Y和Z代表三种不同周期的短周期元素,其原子序数依次增大。且知:X与Y可形成原子个数比分别为1∶1的共价化合物甲和2∶1的共价化合物乙;Y与Z可形成原子个数比分别为1∶1的离子化合物丙和2∶1的离子化合物丁。请回答:
Y和Z代表三种不同周期的短周期元素,其原子序数依次增大。且知:X与Y可形成原子个数比分别为1∶1的共价化合物甲和2∶1的共价化合物乙;Y与Z可形成原子个数比分别为1∶1的离子化合物丙和2∶1的离子化合物丁。请回答:
(1)元素Y在周期表中的位置为:第周期、第族。
(2)化合物甲的结构式是。
(3)化合物丙中的化学键类型有。
(4)Y的阴离子半径与Z的阳离子半径大小关系为:r(Yn-)r(Zm+)。
A、B、C均为短周期元素,在元素周期表中的相对位置如下图所示,A、C两种元素的原子核外电子数之和等于B原子的核电荷数。请完成下列填空: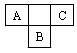
(1)A的原子结构示意图为,A的最高价氧化物对应水化物的的分子式为。
(2)B的简单离子的电子式为。
(3)用电子式表示C的氢化物分子的形成过程: 。
。
(4)C单质与水反应的化学方程式为。
下表列出了A~R等9种元素在元素周期表中的位置:
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
E |
F |
||||||
| 3 |
A |
C |
D |
G |
R |
|||
| 4 |
B |
H |
请按要求用相应的化学用语回答下列问题:
(1)写出下列元素的元素符号:A;E;G。
(2)上述9种元素中,性质最不活泼的元素的一种同位素的原子核内有20个中子,则表示该同位素原子的符号为。
(3)A、C、 D三种元素按金属性由强到弱的顺序排列为。
D三种元素按金属性由强到弱的顺序排列为。
(4)F单质的电子式为。
(5)D元素的最高价氧化物对应的水化物与KOH溶液反应的离子方程式为
。
关于元素周期表的第三周期元素,请用相应的元素符号或化学式回答:
(1)除稀有气体外,原子半径最大的元素是。
(2)非金属性最强的元素是;金属性最强的元素的。
(3)最高价氧化物对应的水化物中,呈两性的物质的化学式为。
(4)最高价氧化物对应的水化物中,碱性最强的物质的化学式为。