在一定体积的密闭容器中放入3升气体R和5升气体Q,在一定条件下发生反应:2R(g)+5Q(g) 4X(g)+nY(g)。反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是:( )
4X(g)+nY(g)。反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是:( )
| A. 2 | B.3 | C.4 | D.5 |
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示。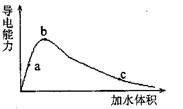
则下列说法错误的是()
| A.醋酸的电离度:c<b<a |
| B.溶液的PH值:b<a<c |
| C.蘸取a点溶液滴在湿润的PH试纸上,测得PH值一定偏大 |
| D.若分别取a、b、c三点的溶液各10mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a>b>c |
下列变化规律中正确的是()
| A.金属Na、Mg、A1溶沸点由高到低 |
| B.HC1、HBr、HI的还原性由弱到强 |
| C.H+、Li+、H-的半径由小到大 |
| D.同浓度的甲酸钠、乙酸钠、碳酸钠溶液的碱性由强到弱 |
金属镁溶于一定浓度的硝酸的反应中,产生标准状下的N2O气体5.6L,在所得的溶液中加入适量的氢氧化钠溶液,完全反应后过滤出沉淀,经洗涤并充分灼烧,最后得到固体物质的质量为
| A.58g | B.29g | C.40g | D.20g |
下列在实验室使用常用玻璃仪器制取有关气体的反应原理正确的是()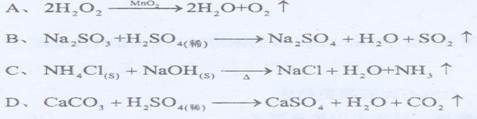
常温下,某水溶液中水的电离度为1.8×10-12%,该溶液不可能是()
| A.烧碱溶液 | B.碳酸氢钠溶液 | C.硝酸溶液 | D.硫酸氢钠溶液 |