下列描述中,不符合生产实际的是( )
| A.电解熔融的氧化铝制取金属铝,用铁作阳极 |
| B.电解法精炼粗铜,用纯铜作阴极 |
| C.电解饱和食盐水制烧碱,用涂镍碳钢网作阴极 |
| D.在镀件上电镀锌,用锌作阳极 |
FeCO3与砂糖混用可以作补血剂,实验室里制备FeCO3的流程如图所示。下列说法错误的是()
| A.可利用KSCN溶液检验FeSO4溶液是否变质 |
| B.沉淀过程中有CO2气体放出 |
| C.过滤搡作的常用玻璃仪器有烧杯、漏斗和玻璃棒 |
| D.产品FeCO3在空气中高温分解可得到纯净的FeO |
下列变化中可以说明SO2具有漂白性的是()
| A.SO2通入高锰酸钾酸性溶液中红色褪去 |
| B.SO2通入品红溶液中红色褪去 |
| C.SO2通入溴水溶液中红棕色褪去 |
| D.SO2通入氢氧化钠与酚酞的混合溶液中红色褪去 |
固体粉末X中可能含有FeO、Fe2O3、MnO2、K2SiO3、K2SO3、KAlO2、MgCl2、K2CO3、NaNO2中的若干种。为确定该固体粉末的成分,现取X进行连续实验,实验过程及产物如图所示:
根据上述实验,以下说法正确的是()
| A.溶液甲中一定含有K2SiO3、NaNO2 |
| B.无法判断溶液中是否有K2SO3 |
| C.气体A和气体B-定为混合物 |
| D.原混合物中一定有Fe2O3 |
已知CN﹣(氢氰酸根离子)SCN﹣(硫氰酸根离子)和Cl﹣有相似之处:两个﹣CN原子团或两个﹣SCN原子团可分别构成氰分子(CN)2和硫氰分子(SCN)2。(CN)2和(SCN)2的性质和Cl2有性质有相似之处,且常温常压下是气体,下列物质间反应的化学方程式错误的是()
A.二氧化锰和HSCN溶液加热反应:MnO2+4HSCN Mn(SCN)2+(SCN)2↑+2H2O Mn(SCN)2+(SCN)2↑+2H2O |
| B.(CN)2和氢氧化钾溶液反应:(CN)2+2KOH═KCN+KCNO+H2O |
| C.碘晶体投入HCN溶液中:I2+2HCN═2HI+(CN)2 |
D.(SCN)2和水反应:(SCN)2+H2O HSCN+HSCNO HSCN+HSCNO |
实验室用含有杂质(FeO、Fe2O3)的废CuO制备胆矾晶体,经历了下列过程(已知 Fe3+在pH=5时沉淀完全)。其中分析错误的是()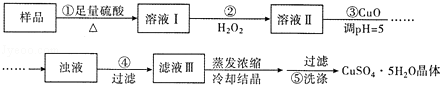
| A.步骤②发生的主要反应为:2Fe2++H2O2+2H+=2Fe3++2H2O |
| B.步骤②可用氯水、硝酸等强氧化剂代替H2O2 |
| C.步骤③用 CuCO3代替CuO也可调节溶液的pH |
| D.步骤⑤的操作为:向漏斗中加人少量冷的蒸馏水至浸没晶体,待水自然流下,重复操作2-3次 |