已知下列热化学方程式:
Zn(s)+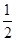 O2(g)==="ZnO(s)" ΔH1=-351.1 kJ/mol Hg(l)+
O2(g)==="ZnO(s)" ΔH1=-351.1 kJ/mol Hg(l)+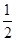 O2(g)==="HgO(s)" ΔH2=-90.7 kJ/mol
O2(g)==="HgO(s)" ΔH2=-90.7 kJ/mol
由此可知Zn(s)+HgO(s)===ZnO(s)+Hg(l)ΔH3,其中ΔH3的值是( )
| A.-441.8 kJ/mol | B.-254.6 kJ/mol | C.-438.9 kJ/mol | D.-260.4 kJ/mol |
25℃、101kPa 下:①2Na(s)+1/2O2(g)=Na2O(s) △H1=-414KJ/mol
②2Na(s)+O2(g)=Na2O2(s) △H2=-511KJ/mol
下列说法正确的是()
| A.①和②产物的阴阳离子个数比不相等 |
| B.①和②生成等物质的量的产物,转移电子数不同 |
| C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
| D.25℃、101kPa下,Na2O2(s)+2Na(s)=2Na2O(s)△H=-317kJ/mol |
在2A(g)+B(g) 3C(g)+4D(g)反应中,表示该反应速率最快的是()
3C(g)+4D(g)反应中,表示该反应速率最快的是()
A.v(A)="0.3mol/L·" sB.v(B)="0.3mol/L·" s
C.v(C)="0.3mol/L·" s D.v(D)="1mol/L·" s
有6.4 g CuO、Fe2O3混合物跟足量CO充分反应后固体减少了1.44 g,反应后全部气体用0.7 mol/L Ba(OH)2溶液100 mL吸收。下列有关叙述中正确的是()
| A.反应中生成的CO2体积为2.016 L |
| B.吸收CO2后的溶液中一定有Ba(HCO3)2 |
| C.不能确定原混合物中CuO与Fe2O3质量比 |
| D.若将质量相同的混合物加过量硝酸溶解后,再加入100 mL的NaOH溶液时沉淀达最大量,由此可求得c(NaOH)=1.8 mol/L |
用一种阴、阳离子双隔膜三室电解槽处理废水中的NH4+,模拟装置如图所示。下列说法正确的是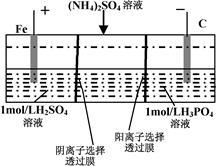
| A.阳极室溶液由无色变成棕黄色 |
| B.阴极的电极反应式为:4OH–-4e–=2H2O+O2↑ |
| C.电解一段时间后,阴极室溶液中的pH升高 |
| D.电解一段时间后,阴极室溶液中的溶质一定是(NH4)3 PO4 |
下列各表述与示意图一致的是()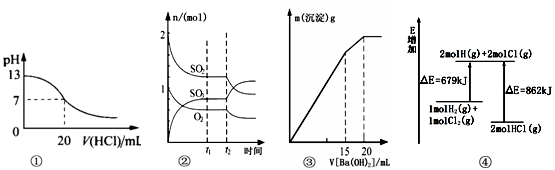
| A.图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入酸体积的变化得到的滴定曲线 |
B.图②表示一定条件下进行的反应2SO2(g) + O2(g) 2SO3(g) ΔH < 0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积 2SO3(g) ΔH < 0各成分的物质的量变化,t2时刻改变的条件可能是降低温度或缩小容器体积 |
| C.图③表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
| D.图④表示化学反应H2(g)+C12(g)==2HCl(g)的能量变化,则该反应的反应热△H=﹢183 kJ/mol |