煤作为燃料,可以有下列两种途径(把煤看成由碳组成):
途径Ⅰ:C(s)+O2(g)===CO2(g) ΔH=-a kJ·mol-1
途径Ⅱ:C(s)+H2O(g)===CO(g)+H2(g) ΔH=+b kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH=-c kJ·mol-1 2H2(g)+O2(g)===2H2O(g) ΔH=-d kJ·mol-1
试回答下列问题:
(1)燃烧等质量的煤,途径Ⅰ放出的热量____途径Ⅱ放出的热量(填“大于”、“小于”或“等于”)。
(2)b的数学关系式是______________(用a、c、d表示)。
(3)由于制取水煤气反应中,反应物具有的总能量________(填“大于”、“小于”或“等于”)生成物所具有的总能量,在反应时,反应物需要______(填“吸收”或“放出”)能量才能转化为生成物。
(4)简述煤通过途径Ⅱ作为燃料的意义__________________________________________________。
聚乙烯醇Z是具有广泛用途的合成高分子材料,结构简式为 ,其工业合成路线如下:
,其工业合成路线如下:
已知:下列反应中R,R',R"代表烃基
i. 
ii. 
回答下列问题:
(1)乙炔的空间构型是____________;
(2)X的结构简式是_____________________;
(3)Y转化为Z的化学方程式是_____________________;
(4)在一定条件下,也可用乙烯、氧气和乙酸制取X,该反应的化学方程式是________________;
(5)已知:
在横线上填入物质、在方框内填上系数完成聚乙烯醇转化为维纶的化学方程式。
3-苯基丙烯醛是一种被广泛应用在食品加工中的高效低毒食品添加剂,下列是用其合成聚酯F的路线示意图: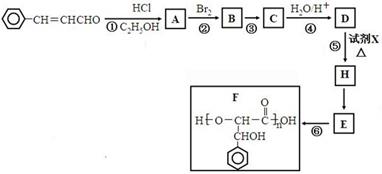
已知:
根据题意回答:
(1)3-苯基丙烯醛分子中官能团的名称为 ;
(2)E的结构简式为 ;
(3)合成路线中的①、④两个步骤的目的是 。
(4)反应③的化学方程式为 。
(5)若X为银氨溶液,则反应⑤的化学方程式为 。
(6)同时符合下列条件的D的同分异构体共有 种。
a.既可发生银镜反应又可发生水解
b.能与FeCl3溶液发生显色反应
c.是苯的二取代物。
上述同分异构体中,核磁共振氢谱有6组峰的结构简式 。 (任写一种)
(7)已知羟醛缩合反应 ,现以甲苯和乙醛为原料制备3-苯基丙烯醛
,现以甲苯和乙醛为原料制备3-苯基丙烯醛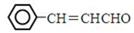 ,设计合成线路(其无机试剂任选),合成线路示意图示例如下:
,设计合成线路(其无机试剂任选),合成线路示意图示例如下:
对叔丁基苯酚 工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯(CH3)3CCl等为原料制备对叔丁基苯酚。实验步骤如下:
工业用途广泛,可用于生产油溶性酚醛树脂、稳定剂和香料等。实验室以苯酚、叔丁基氯(CH3)3CCl等为原料制备对叔丁基苯酚。实验步骤如下: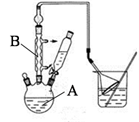
步骤l:组装仪器,用量筒量取2.2 mL叔丁基氯(过量),称取1.6 g苯酚,搅拌使苯酚完全溶解,并装入滴液漏斗。
步骤2:向A中加入少量无水AlCl3固体作催化剂,打开滴液漏斗旋塞,反应有气体放出。
步骤3:反应结束后,向A中加入8 mL水和1 mL浓盐酸,即有白色固体析出。
步骤4:抽滤得到白色固体,洗涤,得到粗产物,用石油醚重结晶,得对叔丁基苯酚1.8 g。
(1)仪器A和B的名称分别为 ; 。
(2)步骤2中发生主要反应的化学方程式为 。该反应为放热反应,且实验的产率通常较低,可能的原因是 。
(3)图中倒扣漏斗的作用是 。苯酚有腐蚀性,能使蛋白质变性,若其溶液沾到皮肤上可用 洗涤。
(4)步骤4中用石油醚重结晶提纯粗产物,试简述重结晶的操作步骤:
(5)实验结束后,对产品进行光谱鉴定,谱图结果如下图。该谱图是 (填字母)。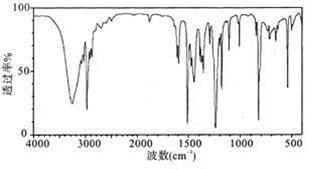
A.核磁共振氢谱图 B.红外光谱图 C.质谱图
(6)下列仪器在使用前必须检查是否漏液的是 (填选项字母)。
A量筒 B容量瓶 C滴定管 D分液漏斗 E长颈漏斗
(7)本实验中,对叔丁基苯酚的产率为 (请保留三位有效数字)。
维拉佐酮是临床上使用广泛的抗抑郁药,其关键中间体合成路线如下:
已知:
回答下列问题:
(1)反应类型:①________________④________________
(2)A和D的结构简式分别为:________________;________________
(3)写出反应②的化学方程式:_________________。实验中反应②在K2CO3弱碱性条件下进行的原因是:____________。
(4)同样具有三个支链,且支链结构与B完全相同,属于芳香族化合物的B的同分异构体一共有________种(不包括B)
(5)反应⑥中(Boc)2O是由两分子羧酸C5H10O3脱水形成的酸酐,且(Boc)2O分子中氢原子化学环境只有1种,写出(Boc)2O的结构简式:
(6) 实验室还可用 和
和  直接反应生成E,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式________。
直接反应生成E,但实验中条件控制不当会发生副反应生成副产物,写出副产物有机物的结构简式________。
已知两个醛分子在NaOH溶液作用下可以发生加成反应,生成一种羟基醛: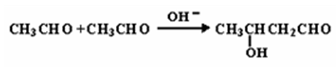
肉桂醛F(分子式为C9H8O)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的
已知:反应⑥为含羟基的物质在浓硫酸催化作用下分子内脱水的反应。反应⑤为碱性条件下醛醛加成反应,请回答
(1)肉桂醛F的结构简式为:________________。E中含氧官能团的名称为________________。
(2)写出下列转化的化学方程式:
②_________________。
③_________________。
写出有关反应的类型:①________________,④________________。
(3)符合下列要求的E物质的同分异构体有种(苯环上有两个取代基,其中有一个甲基在对位且属于酯类)。