(1) 由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式: _ 。
若1g水蒸气转化成液态水放热2.444kJ,则氢气的燃烧热为_____________。
(2)已知①CO(g) + 1/2 O2(g) = CO2(g) ; ΔH1= -283.0 kJ/mol
②H2(g) + 1/2 O2(g) = H2O(l) ; ΔH2= -285.8 kJ/mol
③C2H5OH(l) + 3 O2(g) = 2 CO2(g) + 3H2O(l); ΔH3="-1370" kJ/mol
试写出一氧化碳与氢气反应生成液态水和乙醇液体的热化学方程式:
___________________________________________________________。
(3)Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K,测得在不同
FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K,测得在不同
温度下,K值如下:
| 温度/℃ |
500 |
700 |
900 |
| K |
1.00 |
1.47 |
2.40 |
①若500℃时进行反应,CO2起始浓度为2 mol·L-1,CO的平衡浓度为________。
②此反应焓变中的a________0(填大于、小于、等于)。
根据反应8NH3 + 3Cl2 ="=" 6NH4Cl+ N2 ,回答下列问题:
(1) 还原剂是(写化学式);
(2) 用双线桥法表示该反应电子转移的方向和数目;
(3)当反应中转移1.806×1024个电子时,被氧化的气体在标准状况下的体积为升。
某中学环境监测兴趣小组的同学在一条鱼虾绝迹的小河边发现甲、乙、丙、丁四个工厂 ,如右图所示。这些工厂往小河里排放的废水中各含一种化合物。经检测发现:①甲处河水呈浅黄色;②乙处河水呈红褐色浑浊状;③丙处河水逐渐变澄清;④丁处河水不断冒气泡;⑤M处水样的pH大于7,加入足量的稀HNO3后再加入BaCl2溶液,无沉淀生成; ⑥N处水样的 pH小于7。请回答: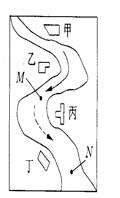
(1)四个工厂所排放的废水中,分别含有下列化合物中的哪种物质:
硫酸铁、氢氧化钠、硝酸银、碳酸钠、氯化铁、硫酸。
甲______,乙______,丙______,丁______。(均填化学式)
(2)写出丙、丁两处所发生反应的离子方程式:
丙_______________; 丁_______________。
四只失去标签的试剂瓶中分别盛有NaCl溶液、NaNO3溶液、Na2CO3溶液和Na2SO4溶液,就如何检验这四种溶液做如下实验:先用四只试管分别取四种溶液各1mL, ① 在四只试管中分别滴入过量的同一种试剂,根据反应现象检验出一种物质;② 在剩余的三只试管中分别滴入第二种试剂,又检验出一种物质;③ 在剩余的两只试管中分别滴入第三种试剂,检验出第三种物质;④在三次实验中都没有明显现象的是第四种物质。请回答:
(1)①中加入的试剂的名称是;
(2)②中检验出的物质是(写化学式);
(3)③中反应的现象是。
某同学将标准状况下44.8L的HCl气体溶于水,配成500mL的溶液,并取出100mL该盐酸溶液与2mol/L的Ba(OH)2溶液进行中和反应。
(1)根据公式,可知该HCl气体的物质的量为________。
(2)根据公式,可知所配成的盐酸溶液的物质的量浓度为。
(3)100mL盐酸溶液中含HCl的物质的量为,
(4)根据化学反应方程式,可知反应过程中n[Ba(OH)2]: n(HCl) =,所以n[Ba(OH)2]为mol,因此,反应所消耗的的体积Ba(OH)2为。
纯净物根据其组成和性质可进行如下分类。
(1)上图所示的分类方法属于(填序号)
A.交叉分类法 B.树状分类法
(2)以H、O、S、N、K、Ba六种元素中任意两种或三种元素组成合适的常见物质,分别将其中一种常见物质的化学式填写于下表相应类别中:
| 物质类别 |
酸 |
碱 |
盐 |
氧化物 |
| 化学式 |
(3)从上表酸及碱中各选出一种能相互反应的物质,并写出其反应的化学方程式:
。