某温度时,在10 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化下表中数据
| t/min |
X/mol |
Y/mol |
Z/mol |
| 0 |
1.00 |
2.00 |
0.00 |
| 1 |
0.90 |
1.80 |
0.20 |
| 3 |
0.75 |
1.50 |
0.50 |
| 5 |
0.65 |
1.30 |
0.70 |
| 9 |
0.55 |
1.10 |
0.90 |
| 10 |
0.55 |
1.10 |
0.90 |
| 14 |
0.55 |
1.10 |
0.90 |
(1) 体系中发生反应的化学方程式是____________;
(2) 计算该反应在0~3 min时间内产物Z的平均反应速率:________;
(3) 该反应达到平衡时反应物X的转化率α等于________;
(4) 如果该反应是放热反应,改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1所对应的实验条件改变是:______ ___ ___。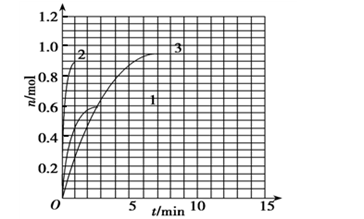
(5)如果起始加入X、Y、Z的物质的量分别为2.00 mol、4.00 mol和0 mol,在原温度下达平衡时,X的转化率为α!,则α! α(填 < > =)。
(6)如果在原温度下起始加入X、Y、Z的物质的量分别为1.00 mol、1.00 mol和1.00 mol,此时可逆反应的反应速率:u(正) u(逆)(填 < > =)。
已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。回答下列问题:
(1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是;
(2)Q的具有相同化合价且可以相互转变的氧化物是;
(3)R和Y形成的二元化合物中,R呈现最高化合价的化合物的化学式是;
(4)这5个元素的氢化物分子中,立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式),其原因是;
(5)电子总数相同的氢化物的化学式和立体结构分别是;
(9分)根据图所示的化学反应框图解题。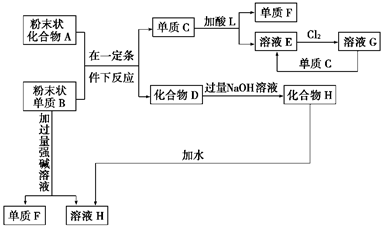
(1)单质F是__________,溶液H中所含的主要离子是_________________________。
(2)写出下列反应的化学方程式:
C+L―→F+E:______,
B―→F+H:______________。
(3)写出下列反应的离子方程式:
E+Cl2―→G:_______________________,
G+C―→E:_______________,
D―→H:__________________________________________。
(4)由C―→E+F若改用浓酸,则不能选用的浓酸是________(填化学式)。
A、B、C、D四种元素都是短周期元素。A元素的离子具有黄色的焰色反应。B元素的离子结构和Ne具有相同的电子层排布;5.8gB的氢氧化物恰好能与100ml 2mol/L盐酸完全反应;B原子核中质子数和中子数相等。H2在C单质中燃烧产生苍白色火焰。D元素原子的电子层结构最外层电子数是次外层电子数的三倍。根据上述条件,回答:
(1)元素C位于第_____周期第_____族,它的最高价氧化物的化学式为______。
(2)A是元素_________,B是元素_________,D是元素____________。
(3)A与D形成稳定化合物的化学式为_____________,判断该化合物在空气是否变质的简易方法是_______________。
(4)C元素的单质有毒,可用A的最高价氧化物对应的水化物的溶液来吸收,其离子方程式为___________________________。
1 molH2O中含有mol e—
0.1molNH4+中约含有个N,约含有个H.