在一个固定体积的密闭容器中,加入2molA和1molB发生反应:2A(g)+B(g)  3C(g)+D(g)达到平衡时,C的浓度为amol/L.若维持容器体积和温度不变,按下列四种配比为起始物质,达平衡后,C的浓度仍为amol/L的是( )
3C(g)+D(g)达到平衡时,C的浓度为amol/L.若维持容器体积和温度不变,按下列四种配比为起始物质,达平衡后,C的浓度仍为amol/L的是( )
| A.4molA + 2mol B |
| B.2molA + 1molB + 3molC + 1molD |
| C.3molC + 1molD + 1molB |
| D.3molC + 1molD |
下列物质哪些与苯酚互为同系物( )
A.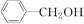 |
B. |
C. |
D.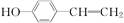 |
柠檬烯是一种食用香料,其结构简式如图。有关柠檬烯的分析正确的是( )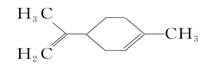
| A.它的一氯代物有6种 |
B.它和丁基苯(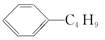 )互为同分异构体 )互为同分异构体 |
| C.它的分子中所有的碳原子一定在同一个平面上 |
| D.一定条件下,它分别可以发生加成、取代、氧化、还原等反应 |
有机物A的结构简式为 ,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )
,A的同分异构体中带苯环的化合物(烯醇结构除外)共有( )
| A.3种 | B.4种 | C.5种 | D.6种 |
下列说法正确的是( )
| A.除去溴苯中的溴,可加入过量的KI溶液后分液 |
| B.葡萄糖、蔗糖都能与新制氢氧化铜浊液发生反应 |
| C.蛋白质水解的最终产物既能和强酸反应,又能和强碱反应 |
| D.纤维素属于高分子化合物,与淀粉互为同分异构体 |
下列实验能获得成功的是( )
| A.将乙醛滴入银氨溶液中,加热煮沸制银镜 |
| B.苯与浓溴水反应制取溴苯 |
| C.向浓溴水中加几滴苯酚观察沉淀 |
| D.1 mol·L-1 CuSO4溶液2 mL和0.5 mol·L-1 NaOH溶液4 mL混合后加入40%的乙醛溶液0.5 mL,加热煮沸观察沉淀的颜色 |