化合反应、分解反应、置换反应、复分解反应与氧化还原反应的交叉分类示意图正确的是()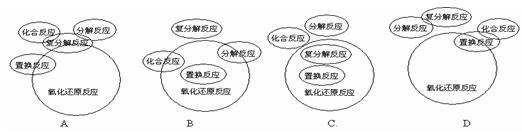
下列各项操作,其中错误的是()
| A.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 |
| B.进行分液时,分液漏斗中的下层液体从漏斗颈下口流出,上层液体则从分液漏斗的上口倒出 |
| C.萃取、分液前需对分液漏斗检漏 |
| D.为保证分液漏斗内的液体顺利流出,需将分液漏斗上口部的塞子打开 |
给150mL某液体加热,操作中所用仪器是:①试管②烧杯③酒精灯④试管夹⑤石棉网⑥泥三角 ⑦坩埚 ⑧铁架台()
| A.③⑥⑦⑧ | B.②③⑤⑧ |
| C.①③④ | D.②③⑤⑥ |
下列反应中,离子方程式书写正确的是()
| A.氢氧化钡与盐酸反应: OH—+H+=H2O |
| B.Fe和盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C.Cu和AgNO3溶液反应:Cu+Ag+=Cu2++Ag |
| D.石灰石和盐酸反应:CO32—+2H+=CO2↑+H2O |
农药波尔多液可用于水果灭虫,是由石灰水和硫酸铜溶液混合而成的悬浊液。它不能用铁制容器盛放,是因为铁与该农药中的硫酸铜起反应。在该反应中,对铁的叙述错误的是()
| A.铁发生还原反应 | B.铁发生氧化反应 |
| C.铁是还原剂 | D.铁失去电子 |