某金属氯化物MCl2 27g,含有0.40molCl-,则该氯化物的物质的量为______,摩尔质量为 ,金属M的相对原子质量为 。
(1)向Na2CO3的浓溶液中逐滴加入稀盐酸,直到不再生成CO2气体为止,则在此过程中,溶液的c(HCO3-)变化趋势可能是:①逐渐减小;②逐渐增大;③先逐渐增大,而后减小;④先逐渐减小,而后增大。4种趋势中可能的是________。
(2)pH相同的HCl溶液、H2SO4溶液、CH3COOH溶液各100 mL。
①分别用0.1 mol /L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
/L的NaOH溶液中和,其中消耗NaOH溶液最多的是________(填化学式)。
②与等量的锌粉反应,反应开始时,反应速率________。
A.HCl最快 B.H2SO4最快 C.CH3COOH最快 D. 一样快
一样快
(3)某温度下,纯水中c(H+)=2×10-7 mol/L,则此时0.02mol/LBa(OH)2溶液的pH =
(4)有四种一元酸HA、HB、HC、H D,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质
D,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大,NaA溶液呈中性,1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质 的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
的量浓度的HB、HC用样的装置分别作导电性试验,发现后者的灯泡比前者亮,则这四种酸的酸性由强到弱的顺序为________________________。
铅蓄电池是典型的可充型电池,它的正负极板是惰性材料,电池总反应式为:
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是___________________________;电解质溶液中H2SO4的浓度将_______ (填“变大”、“变小”或“不变”);当外电路通过1 mol电子时,理论上负极板的质量增加_______ g。
(2)在完全放电耗尽PbO2和Pb时,若按图连接,电解一段时间后,则在A电极上生成____________、B电极上生成______________,此时铅蓄电池的正负极的极性将_______________________。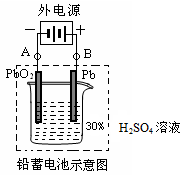
下图中每一方框中的字母代表一种反应物或生成物(部分产物未列出):
已知C是紫红色金属固体,B的浓溶液和稀溶液都是有强氧化性。
(1)A的化学式是,E化学式是;
(2)电解反应的化学(或离子)方程式是;
(3)对200ml 1mol/L的A溶液进行电解,当有0.02mol电子发生转移时,溶液的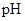 为
为
(假设溶液体积不变)。
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化,据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是。
(2) 根据上述框图反应关系,写出下列B、D所含物质的化学式
根据上述框图反应关系,写出下列B、D所含物质的化学式
固体B;沉淀D
(3)写出①、②、两个反应的离子方程式
①
②
现有三种物质A、B、C,它们均溶于水。其中有一种是酸,一种是碱,一种是盐,溶于水后电离,可以产生下表中的离子:
| 阳离子 |
Na+H+Ba2+ |
| 阴离子 |
OH- CO SO SO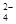 |
为鉴别它们,分别完成以下实验,其结果如下:
① A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
② B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝 酸。
酸。
请根据上述实验结果,填空:
(1)写出下列物质的化学式:X
(2)B溶于水后的电离方程式为
(3)鉴别B中阴离子的实验操作方法是
(4)B与C反应的离子方程式: