溴化碘(IBr)的化学性质与卤素单质相似,能跟大多数金属反应生成金属卤化物,能跟水反应IBr+H2O==HBr+HIO.下列有关叙述中不正确的是
| A.IBr是双原子分子 |
| B.IBr与水反应时,它既是氧化剂,又是还原剂 |
| C.在很多化学反应中IBr作氧化剂 |
| D.跟NaOH溶液反应可生成NaBr和NaIO |
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。有关说法不正确的是( )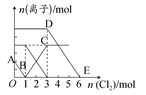
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中c(FeBr2)=6 mol·L-1 |
| C.当通入Cl22 mol时,溶液中已发生的离子反应可表示为:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3 |
将1.12 g铁粉加入25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是( )
| A.铁有剩余,溶液呈浅绿色,Cl-浓度基本不变 |
| B.往溶液中滴入无色KSCN溶液,显黄色 |
| C.Fe2+和Fe3+的物质的量之比为6:1 |
| D.氧化产物与还原产物的物质的量之比为2:5 |
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2.24 L NO,剩余9.6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下2.24 L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法正确的是( )
| A.原混合物中铜和铁各0.15 mol |
| B.稀硝酸的物质的量浓度为1 mol/L |
| C.第一次剩余的9.6 g金属为铜和铁 |
| D.再加入上述200 mL稀硝酸,还能得到标准状况下2.24 L NO |
下列实验中,溶液颜色有明显变化的是( )
| A.少量明矾溶液加入到过量NaOH溶液中 |
| B.往FeCl3溶液中滴入KI溶液,再滴入淀粉溶液 |
| C.少量Na2O2固体加入到过量NaHSO4溶液中 |
| D.往酸性高锰酸钾溶液中滴入少量Fe2(SO4)3稀溶液 |
A、B、C、X均为中学化学常见物质,一定条件下它们有如图转化关系(其他产物已略去),下列说法正确的是( )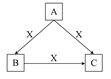
A.若X为Fe,则C可能为Fe(NO3)2
B.若X为KOH溶液,则A可能为Al
C.若A、B、C均为焰色反应呈黄色的化合物,则X一定为CO2
D.若X为O2,则A可为有机物乙醇,也可为非金属单质硫