条件一定时,反应2A(g)+B(g) 2C(g),B的转化率α与温度T变化关系曲线图如下所示,图中4个点中,表示未达到平衡状态,且V正<V逆的点是
2C(g),B的转化率α与温度T变化关系曲线图如下所示,图中4个点中,表示未达到平衡状态,且V正<V逆的点是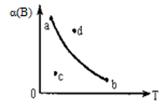
| A.a | B.b | C.c | D.d |
在密闭容器中进行反应X2(g)+Y2(g) 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.1 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.1 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
| A.Y2为0.1 mol·L-1 | B.X2为0.1 mol·L-1 |
| C.Y2为0.35 mol·L-1 | D.Z为0.3 mol·L-1 |
将1 mol冰醋酸加入到一定量的蒸馏水中最终得到1 L溶液。下列各项中,表明已达到电离平衡状态的是
| A.醋酸的浓度达到1 mol·L-1 |
| B.H+的浓度达到0.5 mol·L-1 |
| C.醋酸分子的浓度、醋酸根离子的浓度、H+的浓度均为0.5 mol·L-1 |
| D.醋酸分子电离成离子的速率和离子重新结合成醋酸分子的速率相等 |
下列说法可以证明反应N2(g)+3H2(g) 2NH3(g)已达到平衡状态的是
2NH3(g)已达到平衡状态的是
| A.1个N≡N键断裂的同时,有3个H—H键形成 |
| B.1个N≡N键断裂的同时,有3个H—H键断裂 |
| C.N2、H2、NH3的分子数之比为1∶3∶2 |
| D.1个N≡N键断裂的同时,有6个H—N键形成 |
中和热是在稀溶液中,强酸、强碱发生中和反应生成1 mol水时放出的热量,中和热为57.3 kJ/mol。下列热化学方程式中正确的是
| A.HNO3(aq)+KOH(aq)===H2O(l)+KNO3(aq) ΔH>-57.3 kJ/mol |
| B.HNO3(aq)+NH3·H2O(aq)===H2O(l)+NH4NO3(aq)ΔH<-57.3 kJ/mol |
| C.CH3COOH(aq)+KOH(aq)===H2O(l)+CH3COOK(aq) ΔH<-57.3 kJ/mol |
| D.CH3COOH(aq)+NH3·H2O(aq)===H2O(l)+CH3COONH4(aq) ΔH>-57.3 kJ/mol |
下列说法中正确的是
| A.ΔH>0表示放热反应,ΔH<0表示吸热反应 |
| B.反应产物的总焓大于反应物的总焓时,ΔH>0 |
| C.ΔH的大小与热化学方程式中的各物质的化学计量数无关 |
| D.在化学反应中,发生物质变化的同时不一定发生能量变化 |