甲醇(CH3OH)是一种可再生能,具有开发和应用的广阔前景,工业上一般可采用如下反应合成甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(1)t℃时,往1L密闭容器中充入1mol CO和2molH2。10min后,反应达到平衡,并测得CH3OH(g)的浓度为0.8 mol·L-1。
①该时间内反应速率v(H2) =____。t℃时,该反应的化学平衡常数K= (mol·L-1)-2
②下列各项中,能说明该反应已达到平衡的是_____________(填序号)
a.恒温、恒容条件下,容器内的压强不发生变化
b.一定条件下,测得v正(CO) =v逆(CH3OH)
c.恒温、恒容条件下,容器内的气体密度不发生变化
d.一定条件下,单位时间内消耗2 mol H2,同时生成1 mol CH3OH(g)
(2)下图是该反应在T1 、T2温度下CO的转化率随时间变化的曲线。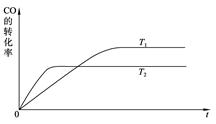
①该反应的焓变ΔH____0(填“>”、“<”或“=”)。
②T1和T2温度下的平衡常数大小关系是K1____________K2(填“>”、“<”或“=”)。
③若保持容器容积不变,下列措施可增加甲醇产率的是______________。
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH =-a kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH =-b kJ·mol-1
则,CH3OH(l)+O2(g) =CO(g)+2H2O(g) ΔH=____________kJ·mol-1。
(4)我国在甲醇燃料电池技术方面已获得重大突破。甲醇燃料电池的工作原理如图所示。
①该电池工作时,b口通入的物质为______。
②该电池正极的电极反应式为 。
学习化学要准确掌握化学基本概念和研究方法。按要求回答下列问题:
(1)下列是某同学对有关物质进行分类的列表:
找出上述三组分类中的错误,错误物质的化学式为 。
(2)下列2个反应,按要求填写相关量。
①2Na2O2+ 2H2O=4NaOH+O2反应中,每消耗lmol Na2O2生成 g O2;
②除去NaCl溶液中少量的Na2SO4杂质,要判断所加BaCl2溶液是否过量,可向滤液中加入X溶液,X可以是 (填代号)
A.NaOHB.AgNO3C.HClD.Na2SO4
(3)配平下面化学方程式,回答下列问题:
①H2SO4在上述反应中表现出来的性质是(填选项编号) .
A.氧化性B.氧化性和酸性C.酸性D.还原性和酸性
②若反应中电子转移了0.8 mol,则产生的气体在标准状况下的体积为_____L。
(4)在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,按要求回答下列问题:
该变化的基本反应类型是 反应,Q物质的作用为 。
【选修3--物质结构与性质)铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途.
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
①Cu2+的价电子排布图 ;
NH4CuSO3中N、O、S三种元素的第一电离能由大到小顺序为 (填元素符号).
②SO42﹣的空间构型为 ,SO32﹣离子中心原子的杂化方式为 .
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式: 。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4•H2O晶体.
①下列说法正确的是
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因 。
(4)FeO晶胞结构如图所示,FeO晶体中Fe2+配位数为________,若该晶胞边长为acm,则该晶体密度为 。
【化学——选修有机化学基础】呋喃酚是合成农药的重要中间体,其合成路线如下:
(1)A物质核磁共振氢谱共有 个峰,B→C的反应类型是 。
(2)已知X的分子式为C4H7C1,写出A→B的化学方程式: 。
(3)Y是X的同分异构体,分子中无支链且不含甲基,则Y的名称(系统命名)是 。
(4)下列有关化合物C、D的说法正确的是 。
①可用氯化铁溶液鉴别C和D ②C和D含有的官能团完全相同
③C和D互为同分异构体 ④C和D均能使溴水褪色
(5)E的同分异构体很多,写出两种符合下列条件的芳香族同分异构体的结构简
式: 、 。
①环上的一氯代物只有一种
②含有酯基
③能发生银镜反应
运用相关原理,回答下列各小题:
(1)25℃时,某FeCl3溶液的pH=2,则此溶液中由水电离产生的c(OH-)= ;用离子方程式表示FeCl3溶液用于净水的原因: 。
(2)已知Ksp(AgCl)=1.8×10﹣10,若向50mL0.018mol•L﹣1的AgNO3溶液中加50mL 0.020mol•L﹣1的盐酸,混合后溶液中Ag+的浓度为 。
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛。现向100 mL 0.1 mol·L-1NH4HSO4 溶液中滴加0.1 mol·L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是_________;
②其溶液中c(OH-)的数值最接近NH3·H2O的电离常数K数值的是 ;
③在c点,溶液中各离子浓度由大到小的排列顺序是 。
利用LiOH和钴氧化物可制备锂离子电池正极材料.LiOH可由电解法制备,钴氧化物可通过处理钴渣获得.
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.B极区电解液为 溶液(填化学式),阳极电极反应式为 ,电解过程中Li+向 电极迁移(填“A”或“B”).
(2)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:
Co(OH)3溶解还原反应的离子方程式为 ,铁渣中铁元素的化合价为 ,在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为 。