下列离子方程式中不正确的是
| A.FeBr2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl- |
| B.将氧气通入酸性碘化钾溶液中:2I-+O2+4H+=I2+2H2O |
| C.硫代硫酸钠溶液中加入稀硫酸:2H++S2O32-=S↓+SO2↑+H2O |
| D.酸性高锰酸钾溶液中加入草酸:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O |
向NaOH和Na2CO3混合溶液中滴加0.1mol/L稀盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示。下列判断正确的是 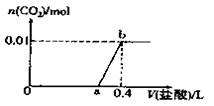
| A.在0-a范围内,只发生中和反应 |
| B.ab段发生反应的离子方程式为:CO32-+2H+=H2O+CO2↑ |
| C.a=0.3 |
| D.原混合溶液中NaOH与Na2CO3的物质的量之比为1:2 |
X、Y、Z、W有如图所示的转化关系,则X、Y可能是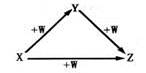
①C、CO②AlCl3Al(OH)3③N2、NO④S、SO2
A.②③B.①②C.③④D.①④
下表为元素周期表前四周期的一部分,其中R为稀有气体元素,下列有关X、W、Y、R、Z(X、W、Y、R、Z分别代表元素符号)五种元素的叙述中,正确的是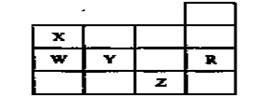
| A.常温常压下,五种元素的单质中有两种是气态 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物比X的氢化物稳定 |
| D.Y与W元素的最高价氧化物对应的水化物的酸性比较,前者弱于后者 |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.在0.1 mol·L-1 NaOH溶液中:K+、Na+、SO42-、HCO3- |
| B.在0.1 mol·L-1 Na2CO3溶液中:Al3+、Ba2+、NO3-、Cl- |
| C.在0.1 mol·L-1 FeCl3溶液中:K+、NH4+、I-、SCN- |
| D.在c( H+)/c(OH-)=10-12的溶液中:K+、Na+、ClO-、NO3- |
下列说法不正确的是
| A.浓硫酸具有强氧化性,但SO2气体可以用浓硫酸干燥 |
| B.常温下实验室可以用稀硝酸与铁反应制取NO气体 |
| C.从海水中提取溴的过程中常鼓入热空气,其目的是氧化Br- |
| D.SiO2不仅能与氢氧化钠溶液反应,也能与氢氟酸反应 |