实验室需要0.5 mol·L-1硫酸溶液480 ml。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液需要的是______(填序号),在使用如下B、C两种仪器前都应进行的操作 。
(2)下列操作中,容量瓶所不具备的功能有______ __(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
(3)根据计算,用量筒量取18.4 mol·L-1的浓硫酸体积为___ ___ ml, 如果实验室有10 mL、15 mL、20 mL量筒,选用 ml的量筒最好。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度________0.5 mol·L-1(填“大于”、“等于”或“小于”,下同)。若浓硫酸在烧杯中溶解后,未冷却至室温就转移至容量瓶,则所得溶液浓度________0.5 mol·L-1。
为了有效实现NO和NO2的相互转化,设计如下实验:按图组装好实验装置,并检查装置气密性,实验前用排水法收集半瓶NO气体。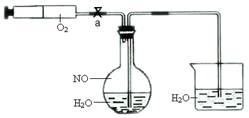
(1)打开止水夹a ,推动针筒活塞,使O2进入平底烧瓶。关上止水夹a ,首先观察到烧瓶中的现象:,
产生此现象的化学反应方程式为:。
(2)轻轻摇动平底烧瓶,观察到烧瓶中的现象为:
①
②
产生此现象的化学反应方程式为 ______________。
1,2 - 二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度2.18 g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂.在实验室中可以用下图所示装置制备1,2-二溴乙烷.其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水). 填写下列空白: 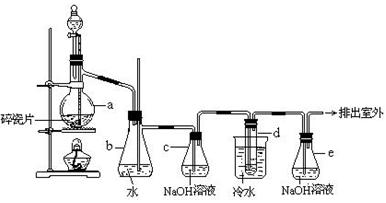
(1)写出本题中制备1,2-二溴乙烷的两个化学反应方程式
_____________________________________、
(2)安全瓶b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞.请写出发生堵塞时瓶b中的现象._________________________________.
(3)容器c中NaOH溶液的作用是:__________________________________.
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多.如果装置的气密性没有问题,试分析其可能的原因(写出一条既可)
___________________________________________________________
在如图所示的实验装置中,当A、B、C分别为以下不同组合时,回答有关问题。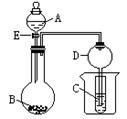
(1)当A为盐酸、B为贝壳(粉末)、C为水玻璃时,小试管中的现象是,其中发生的离子反应方程式是。
(2)当A为浓氨水、B为生石灰、C为AlCl3溶液,小试管中出现的现象是,反应的离子方程式为。
(3)当A为浓硫酸、B为Mg、Al、Fe、Cu中的一种银白色片状金属、C为品红溶液,小试管中溶液红色褪去,则A和B反应的化学方程式是。
(4)装置D的作用是 。
。
化学兴趣小组设计实验,测定Na2CO3与NaHCO3混合物中Na2CO3的质量分数。
甲方案:
实验步骤为:①称量空坩埚的质量为m1g;②称量装有试样的坩埚质量为m2g;③加热;④冷却;⑤称量坩埚和残余物的质量为m3g;⑥重复③至⑤操作,直至恒重,质量为m4g。
(1)坩埚中发生反应的化学方程式为。
(2)计算Na2CO3质量分数必须用到的测定数据为。
乙方案:
在天平上准确称取0.3200g样品,放入锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用0.1000mol·L-1的标准盐酸滴定至溶液由粉红色刚好 变为无色(发生的反应为H++CO2-3=HCO-3)。重复上述操作两次。
变为无色(发生的反应为H++CO2-3=HCO-3)。重复上述操作两次。
(3)根据下表数据,样品中w(Na2CO3)=.
| 滴定次数 |
样品的质量/g |
稀盐酸的体积/mL |
|
| 滴定前刻度/mL |
滴定后刻度/mL |
||
| 1 |
0. 320 320 |
1.02 |
21.03 |
| 2 |
0.320 |
2.00 |
21.99 |
| 3 |
0.320 |
0.20 |
20.20 |
(4)如果滴定后俯视读数,w(Na2CO3)(填“偏高”、“偏低”或“不受影响”)。
丙方案:
称取m g样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
(5)某同学按以下方法检查装置A的气密性:在分液漏斗中加入适量水,如图连接好装置,关闭止水夹a,用止水夹夹住橡皮管c,打开活塞b。若分液漏斗中的水无法持续滴下,试判断装置A是否漏气?(填“漏气”、“不漏气”或“无法确定”)。
(6)为了提高测定的准确性,应选用装置A和(填写字母标号)进行实验。
(7)实验时还需要知道的物理量是。
硫酸是一种实验室常用的化学试剂。请按要求填空:
(1)浓硫酸试剂瓶上适合贴上的图标是(填写字母标号)。
(2)实验室用1.0mol·L-1的硫酸配制0.10mol·L-1的稀硫酸100mL,所需要的玻璃仪器为烧杯、玻璃棒、胶头滴管、酸式滴定管和。
(3)用上图所示的实验装置②验证铜与浓硫酸反应的还原反应,则装置②、③中试剂依次为:、。