A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的P亚层中有4个电子。
(1)D原子的电子排布式为 ,若A元素的原子最外层电子排布为1s1,则按原子轨道的重叠方式,A与C形成的化合物中的共价键属于 键。
(2)当n=2时,B的原子结构示意图为 ,B与C形成的晶体属于 晶体。
当n=3时,B与C形成的晶体属于 晶体。
(3)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,元素A在周期表中的位置是 ,A、B、C、D四种元素的电负性由大到小的顺序是 (用元素符号表示)。
(4)C和D的最简单氢化物相比较:稳定性: (填化学式,下同);
沸点: 原因是 。
以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
C(s)+H2O(g)  CO(g)+H2(g)ΔH=+131.3 kJ•mol-1,
CO(g)+H2(g)ΔH=+131.3 kJ•mol-1,
①该反应在常温下自发进行(填“能”与“不能”);
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有
Ⅰ混合气体的密度;Ⅱ容器内气体的压强;
Ⅲ混合气体的总物质的量;ⅣCO物质的量浓度
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ D.Ⅰ、Ⅲ和Ⅳ
(2)水煤气再进一步反应可制取氢气。反应为H2O(g)+CO(g)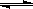 H2(g)+CO2(g),某温度下该反应的平衡常数K= 4/9。该温度下在甲、乙、丙三个恒容密闭容器中,只投入H2(g)和CO2(g),其起始浓度如下表所示。下列判断不正确的是。
H2(g)+CO2(g),某温度下该反应的平衡常数K= 4/9。该温度下在甲、乙、丙三个恒容密闭容器中,只投入H2(g)和CO2(g),其起始浓度如下表所示。下列判断不正确的是。
| 起始浓度 |
甲 |
乙 |
丙 |
| c(H2)/mol/L |
0.010 |
0.020 |
0.020 |
| c(CO2)/mol/L |
0.010 |
0.010 |
0.020 |
A.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
B.平衡时,甲中和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L
D.平衡时,乙中CO2的转化率大于60%
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g)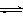 CH3OH(g)+H2O(g) ,右图表示该反应进行过程中能量(单位为kJ•mol—1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2反应
CH3OH(g)+H2O(g) ,右图表示该反应进行过程中能量(单位为kJ•mol—1)的变化。在体积为1 L的恒容密闭容器中,充入1mol CO2和3mol H2反应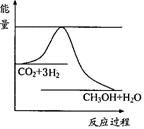
①下列措施中能使c (CH3OH)增大的是。
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出来
D.再充入1mol CO2和3mol H2
②在温度T1时,当反应达到平衡时,测得n(H2) =" 2.4" mol;其它条件不变,在温度T2时,当反应达到平衡时,测得n(CO2) =" 0.82" mol,则T2 T1。(填“>”、“<”或“=”),
(4)在一定条件下科学家从烟道气中分离出CO2与太阳能电池电解水产生的H2合成甲醇。CH3OH、H2的燃烧热分别为:△H=-725.5kJ/mol、△H=-285.8kJ/mol。
①写出工业上以CO2、H2合成CH3OH和液态水的热化学方程式:;
②该转化的积极意义是;
③有人提出,可以设计反应CO2=C+O2(△H>0、△S<0)来消除CO2对环境的影响。请你判断是否可行并说出理由:
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施。化学反应的反应热通常用实验进行测定,也可进行理论推算。
(1) 实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,则甲醇的燃烧热ΔH=。
(2)今有如下两个热化学方程式:则ab(填>, =" ," <)
H2(g)+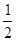 O2(g) = H2O(g) ΔH1=a kJ·mol-1
O2(g) = H2O(g) ΔH1=a kJ·mol-1
H2(g)+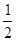 O2(g) = H2O(l)ΔH2=b kJ·mol-1
O2(g) = H2O(l)ΔH2=b kJ·mol-1
(3)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 |
H-H |
N-H |
N≡N |
| 键能/kJ·mol-1 |
436 |
391 |
945 |
已知反应N2(g)+3H2(g)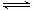 2NH3(g)△H=a kJ·mol-1。试根据表中所列键能数据估算a 的值:(写出 + 或-)。
2NH3(g)△H=a kJ·mol-1。试根据表中所列键能数据估算a 的值:(写出 + 或-)。
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算。
已知:C(s)+O2(g)=CO2(g)△H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ·mol-1
根据盖斯定律,计算298K时由C(s)和H2(g)生成1mol C2H2(g)反应的反应热△H =。
(7分)某含氧有机化合物,它的相对分子质量为88.0,含C的质量分数为68.2%,含H
的质量分数为13.6%,经红外光谱测定含有一个羟基,核磁共振氢谱显示该分子中有3个
甲基,且有三种不同环境的氢原子,
(1)其分子式为______,结构简式为____________。
(2)其同分异构体中与其含有相同官能团的共有___种(不含此有机物,填数字)。
已知A、B、C、D、E都是元素周期表中前36号的元素,其原子序数依次增大。A与其他4种元素既不在同一周期又不在同一族。B和C属同一主族,D和E属同一周期,又知E是周期表中1—18列中的第8列元素。D的原子序数比E小6,D跟B可形成离子化合物其晶胞结构如右图。 请回答:
请回答:
 (1)
(1) A与B形成的化合物在固态时的晶体类型是;A与B形成的化合物
A与B形成的化合物在固态时的晶体类型是;A与B形成的化合物
比A与C形成的化合物熔点要____(填高、低)
(2)
 写出C的单质与水反应的离子方程式;
写出C的单质与水反应的离子方程式;
(3)如图所示,D跟B形成的离子化合物的化学式为;鉴别该离子化合物是否为晶体,最可靠的科学方法是,该离子化合物晶体的密度为ag·cm-3,B、D两元素的相对原子质量分别为b、c,则晶胞的体积是cm3(只要求列出算式)。
(8分)⑴键线式 表示的分子式;名称是。
表示的分子式;名称是。
⑵ 中含有的官能团的名称为。
中含有的官能团的名称为。
⑶用价层电子对互斥理论推测下列分子的空间构型:
SO2 ________; HCHO___________.
⑷重结晶的首要工作是选择适当的溶剂,要求该溶剂:
a.杂质在此溶剂中溶解度______________ 。
b.被提纯的物质在此溶剂中溶解度__________________。