下列叙述不正确的是
| A.将SO2通入BaCl2溶液中至饱和,无沉淀产生;再通入Cl2产生沉淀 |
| B.向AlCl3溶液中加氨水,产生白色沉淀;再加入过量氨水,沉淀消失 |
| C.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO3)2固体,铜粉溶解 |
| D.纯锌与稀硫酸反应产生氢气的速率较慢:再加入少量CuSO4固体,速率加快 |
下列实验操作不正确的是
| A.用倾析法分离时,将烧杯中的上层清液用玻璃棒引流到另一容器内,即可使沉淀与清液分离 |
| B.洗涤沉淀时,应在过滤器中加入洗涤液浸没沉淀,过滤,并重复2到3次 |
| C.抽滤完毕,应先拆下连接抽气泵和吸滤瓶的橡胶管,再关闭水龙头,最后将滤液从吸滤瓶支管口倒出 |
| D.用移液管取液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
下列实验装置的相关描述不正确的是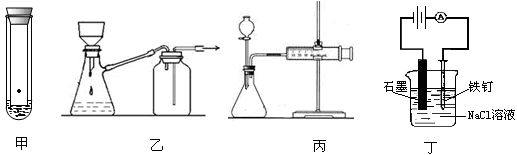
| A.甲装置可用于叶绿体中色素的分离 |
| B.乙装置可用于过滤颗粒很小的沉淀,不宜于过滤胶状沉淀 |
| C.丙装置可用于某些化学反应速率的测定。该装置气密性的检查如下:仪器组装好后,关闭分液漏斗活塞,将针筒活塞向外拉一段距离,然后松手,观察针筒是否能回到原来刻度处 |
| D.丁装置不可用来模拟氯碱工业 |
实验室制备少量硫酸亚铁晶体的实验步骤如下:①趁热过滤②洗涤、滤纸吸干③静置、冷却④水浴加热⑤抽滤⑥过量铁屑,加入20%-30%的稀硫酸溶液。则实验步骤
正确的顺序为
| A.⑥⑤④①③② | B.⑥④⑤②①③ | C.⑥④①③⑤② | D.②⑥④①③⑤ |
用酒精灯加热时,需要垫石棉网的仪器有
①烧杯②坩埚③锥形瓶④蒸发皿⑤试管⑥烧瓶
| A.②④⑤ | B.①②③ | C.④⑤⑥ | D.①③⑥ |
下列各组数据中,前者一定比后者大的是
| A.常温下pH相同的KOH溶液和K2CO3溶液中由水电离出的c(OH-) |
| B.浓度均为0.1mol·L-1的(NH4)2CO3溶液和(NH4)2SO4溶液中的c(NH4+) |
| C.3 L 0.1 mol·L-1CH3COOH溶液和1L 0.3 mol·L-1CH3COOH溶液中的H+离子数 |
| D.中和pH与体积均相同的NaOH溶液和氨水,所消耗H2SO4的物质的量 |