下列反应的离子方程式正确的是
| A.氢氧化铜和盐酸反应:OH-+H+=H2O |
| B.钠和水反应:Na+2H2O=Na++2OH-+H2↑ |
| C.铁和稀硝酸反应:Fe+2H+=Fe2++H2↑ |
| D.常温下,NaOH溶液和Cl2反应:2OH-+Cl2=Cl-+ClO-+H2O |
下列离子方程式书写正确的是()
A.铜溶于浓硝酸:Cu+4HNO3(浓) Cu2++2NO2↑+2H2O Cu2++2NO2↑+2H2O |
B.硫酸铁溶液与氢氧化钡溶液混合:Fe3++S +Ba2++3OH- +Ba2++3OH- Fe(OH)3↓+BaSO4↓ Fe(OH)3↓+BaSO4↓ |
C.次氯酸钙溶液中通入过量的CO2:ClO-+H2O+CO2 HC HC +HClO +HClO |
D.碳酸氢镁与足量的石灰水反应:Mg2++2HC +2OH-+Ca2+ +2OH-+Ca2+ CaCO3↓+MgCO3↓+2H2O CaCO3↓+MgCO3↓+2H2O |
甲、乙两溶液中,分别含有大量的Cu2+、K+、H+、Cl-、C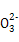 、OH- 6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是()
、OH- 6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是()
A.K+、OH-、C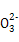 |
B.Cu2+、H+、Cl- |
| C.K+、H+、Cl- | D.C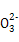 、OH-、Cl- 、OH-、Cl- |
下列表示对应化学反应的离子方程式正确的是()
A.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O Al Al +4N +4N +2H2O +2H2O |
B.用FeCl3溶液腐蚀铜线电路板:Cu+2Fe3+ Cu2++2Fe2+ Cu2++2Fe2+ |
C.大理石溶于醋酸中的反应:CaCO3+2H+ Ca2++H2O+CO2↑ Ca2++H2O+CO2↑ |
D.钠与水反应:Na+2H2O Na++2OH-+H2↑ Na++2OH-+H2↑ |
在熔融KOH中,大气中的氧可将铬铁矿(FeCr2O4)中Fe和Cr的化合价都转化为+6价,氧化1 mol FeCr2O4在理论上需要氧气()
| A.2 mol | B.2.5 mol | C.3 mol | D.4 mol |
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列关于离子共存说法中正确的是()
A.a点对应的溶液中大量存在:Fe3+、Na+、Cl-、S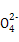 |
B.b点对应的溶液中大量存在:N 、Ba2+、OH-、I- 、Ba2+、OH-、I- |
C.c点对应的溶液中大量存在:Na+、Ba2+、Cl-、HC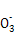 |
D.d点对应的溶液中大量存在:Na+、K+、S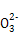 、Cl- 、Cl- |