赤铜矿的成份是Cu2O,辉铜矿的成份是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:2Cu2O+Cu2S 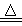 6Cu+SO2↑,对于该反应,下列说法正确的是
6Cu+SO2↑,对于该反应,下列说法正确的是
| A.该反应的氧化剂只有Cu2O |
| B.Cu既是氧化产物又是还原产物 |
| C.每生成1 mol Cu,还原剂转移给氧化剂的电子为2 mol |
| D.该反应中氧化产物与还原产物的质量比为1∶6 |
120 mL含有0.20 mol碳酸钠的溶液和200 mL盐酸,不管将前者滴加入后者,还是将后者滴加入前者,都有气体产生,但最终生成的气体体积不同,则盐酸的浓度合理的是( )
| A.2.0mol/L | B.1.5 mol/L | C.0.18 mol/L | D.0.24mol/L |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系: 。下列有关物质的推断不正确的是( )
。下列有关物质的推断不正确的是( )
| A.若甲为焦炭,则丁可能是O2 | B.若甲为SO2,则丁可能是氨水 |
| C.若甲为Fe,则丁可能是盐酸 | D.若甲为NaOH溶液,则丁可能是CO2 |
已知RxO42-+MnO4-+H+→RO2+Mn2++H2O变化过程中,0.2molRxO42-参加反应,共转移0.4mol电子,则x为()
| A.2 | B.3 | C.4 | D.5 |
下列说法正确的是()
| A.阳离子只能得电子被还原,阴离子只能失电子被氧化 |
| B.已知①Fe+Cu2+=Fe2++Cu;②2Fe3++Cu=2Fe2++Cu2+,则氧化性强弱顺序为: Fe3+>Cu2+>Fe2+ |
| C.化学反应中,得电子越多的氧化剂,其氧化性就越强 |
| D.已知还原性:B->C->D-,反应2C-+D2=2D-+C2和反应2C-+B2=2B-+C2都能发生 |
下列说法正确的是()
| A.萃取溴水中的溴,将四氯化碳和溴水混合后,振荡并打开分液漏斗瓶塞,使漏斗内气体放出 |
| B.在蔗糖中加入浓硫酸时,蔗糖变黑,证明浓硫酸具有脱水性 |
| C.向Ba(NO3)2溶液中通入SO2气体,产生白色沉淀,可推测SO2与可溶性钡盐均能反应产生白色沉淀 |
| D.若要检验铜和浓硫酸反应后产物硫酸铜,可向反应后的试管中加入少量水,观察溶液是否变蓝,若变蓝则证明有硫酸铜生成 |