甲、乙两同学欲分别完成“钠与氯气反应”的实验。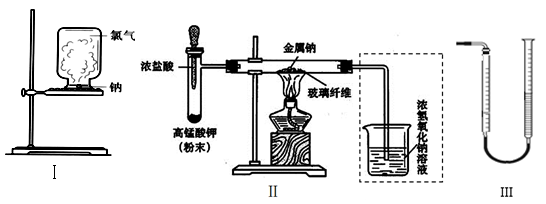
Ⅰ.甲同学的方案为:取一块绿豆大的金属钠(除去氧化层),用滤纸吸净煤油,放在石棉网上,用酒精灯微热。待钠熔成球状时,将盛有氯气的集气瓶抽去玻璃片后倒扣在钠的上方(装置如图Ⅰ)。该方案的不足之处有 。
Ⅱ.乙同学所采用的装置如图Ⅱ,回答下列问题:
(1)按图Ⅱ组装仪器、添加药品,实验开始后,先将浓盐酸挤入试管,试管中发生反应的离子方程式为 ;待整套装置中 后,点燃酒精灯。
(2)点燃酒精灯后,玻璃管中出现的现象是 。
(3)乙同学欲将虚框内装置改为图Ⅲ所示装置,并测量多余气体的体积。
①为提高测量的准确性,图Ⅲ量气管装置中的液体可用 ;收集完气体后并读数,读数前应进行的操作是冷却至室温并 。
②若未冷却至室温立即按上述操作读数,则会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)
③如果开始读数时操作正确,最后读数时俯视右边量气管液面,会导致所测气体的体积__________(填“偏大”、“偏小”或“无影响”)。
甲、乙两同学拟用实验确定某酸HA是弱电解质。他们的方案分别是:
甲:①称取一定质量的HA配制0.1 mol/L的溶液100 mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质。
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100 mL;
②分别取这两种溶液各10 mL,加水稀释为100 mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是。
(2)甲方案中,说明HA是弱电质的理由是测得溶液的pH___1(选填>,<,=)。简要说明pH试纸的使用方法:
(3) 乙方案中,说明HA是弱电解质的现象是_________。
(4)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
一定量的盐酸和过量的锌粒反应产生氢气,为了减慢反应速率,又不影响产生的氢气的总量,下列措施可行的是①加入NaOH固体②加入一定量的水③加入少量硫酸钠溶液④加入少量硫酸铜溶液⑤加入CH3COONa固体⑥加入KNO3溶液。
由金红石(TiO2)制取单质Ti,涉及到的步骤为:
已知:①
②
③
则(1) 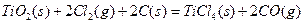 的
的 =________________。
=________________。
(2) 碳在氧气中不完全燃烧生成CO的热化学方程式为__________________________。
21、某同学设计用AlCl3溶液和Na2S溶液反应制取硫化铝(Al2S3)固体,你认为他能达到目的吗?原因是(用离子方程式表示):。配制Na2S溶液时,为了防止水解,常向溶液中加入少量,用离子方程式表示Na2S的水解。
减少SO2的排放、回收利用SO2是环保的重要课题。我国研究人员研制的利用低品位软锰矿浆(主要成分是MnO2)吸收废渣高温焙烧产生的SO2,制备硫酸锰的生产流程如下: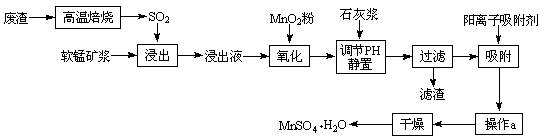
浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其它金属离子。
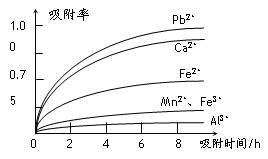
有关金属离子的半径以及形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见下图。
| 离子 |
离子半径(pm) |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe2+ |
74 |
7.6 |
9.7 |
| Fe3+ |
64 |
2.7 |
3.7 |
| Al3+ |
50 |
3.8 |
4.7 |
| Mn2+ |
80 |
8.3 |
9.8 |
| Pb2+ |
121 |
8.0 |
8.8 |
| Ca2+ |
99 |
- |
- |
已知PbO2的氧化性强于MnO2。请回答下列问题:
⑴ 写出浸出过程中主要反应的化学方程式,
氧化过程中主要反应的离子方程式。
⑵ 在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至范围,
滤渣的主要成分有 。
⑶ 阳离子吸附剂用于除去杂质金属离子。决定阳离子吸附剂吸附效果的因素是
(填写序号)。
a.溶液的pHb.金属离子的氧化性c.金属离子的半径d.吸附时间
⑷ 操作a包括过程。