下列指定反应的离子方程式正确的是
| A.NaHCO3溶液中加入醋酸溶液:HCO3-+ H+ = CO2↑+ H2O |
| B.NaAlO2溶液中通入过量CO2气体:2AlO2-+ CO2 +3H2O = 2Al(OH)3↓+CO32- |
| C.Fe(OH)2溶于足量稀硝酸:Fe(OH)2 + 2H+ = Fe2+ + 2H2O |
D.乙醛与含有NaOH的Cu(OH)2悬浊液共热:CH3CHO + OH-+2Cu(OH)2 CH3COO-+ Cu2O↓+3H2O CH3COO-+ Cu2O↓+3H2O |
一定条件下可以大量共存的离子组是
| A.Na+、Fe2+、NO3-、Cl- | B.K+、HCO3-、SO42-、OH- |
| C.ClO-、Cl-、Na+、H+ | D.Ba2+、K+、SO42-、H+ |
某溶液可能含有Clˉ、SO42ˉ、CO32ˉ、NH4+、Fe3+、Fe2+、Al3+和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
由此可知原溶液中
| A.原溶液中c(Fe3+)="0.2" mol·L-1 |
| B.溶液中至少有4种离子存在,其中Clˉ一定存在,且c(Clˉ)≥0.2 mol·L-1 |
| C.SO42ˉ、NH4+、Na+一定存在,CO32ˉ、Al3+一定不存在 |
| D.要确定原溶液中是否含有Fe2+,其操作为:取少量原溶液于试管中,加入足量酸性高锰酸钾溶液,若溶液紫红色褪去,则证明原溶液中有Fe2+ |
下列说法不正确的是
| A.在25℃时,将c mol·L-1的醋酸溶液与0.02mol·L-1NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=2×10—9/(c—0.02) |
| B.0.1 mol·L-1醋酸溶液中:c(H+)2=c(H+)·c(CH3COO一)+KW |
| C.常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO—)与pH值的关系如右图所示,当pH=4.5溶液中:c(CH3COOH)>c(CH3COO—)>c(H+)>c(OH—) |
| D.等体积等物质的量浓度的CH3COONa(aq)与NaCl(aq)中离子总数大小:N前>N后 |
一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g);△H>0。现将1molA和2molB加入甲容器中,将4 molC和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
| A.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| B.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 |
| C.保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
右图是某有机物分子的简易球棍模型,该有机物中中含C、H、O、N四种元素。下列关于该有机物的说法中错误的是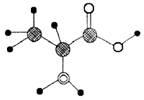
A.分子式为C3H7O2N
B.能发生取代反应
C.能通过聚合反应生成高分子化合物
D.该有机物能跟NaOH溶液反应,但不能和盐酸反应