①标准状况下,甲烷和一氧化碳的混合气体共8.96L,其质量为7.6g,则混合气体中甲烷的体积为 ,一氧化碳的质量为 。
②在标况下气体A的密度为1.25g/L,气体B的相对分子质量为42,A和B的混合气体在相同状况下对H2的相对密度为16.8,则混合气体中A和B的体积比为 。
(8分,多选错选不得分)现有下列物质, 用编号填空回答下列问题:
A.干冰
B.金刚石
C.氦
D.过氧化钠
E.二氧化硅
F.氯化铵
(1)通过非极性键形成的原子晶体是:。
(2)可由原子直接构成的晶体是:。
(3)含有离子键、共价键、配位键的化合物是:。
(4)含有非极性键的离子化合物是:。
(5)已知微粒间的作用力包括离子键、共价键、金属键、范德华力、氢键 。氯化钠熔化,粒子间克服的作用力为____________;二氧化硅熔化,粒子间克服的作用力为____________;干冰气化,粒子间克服的作用力为____________。A、B、C、D四种物质的熔点从低到高的顺序为____________________(填序号)。
A、B、C、D、E五种元素,原子序数依次增大,A、B、C、D属于短周期元素。A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体G,D的L层电子数等于K、M两个电子层上的电子数之和。E、C同族且相邻。根据以上内容,回答下列问题
(1)A为,B为,D为。(填写相应的元素符号)。
(2)写出A、B的化合物与G反应的化学方程式并用双线桥表示出电子转移的方向和数目。
(3)比较B、C简单离子的半径大小:>。
(4)做E元素的焰色反应时,必须透过观察火焰的焰色,其颜色为色。
下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0族 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|||
| 4 |
⑨ |
⑩ |
(1)在这些元素中,化学性质最稳定的是(填元素符号)。最活泼的金属是(填元素符号),离子结构示意图为_________。元素⑩名称为,在周期表中的位置是。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______。
(3)这些元素中能形成两性氢氧化物的元素是(填名称),写出该元素的氢氧化物与④的最高价氧化物的水化物反应的离子方程式。
(4)元素①、②的最简单氢化物的稳定性:大于。(填写氢化物的分子式)
(5)请设计一个实验方案,比较⑥、⑦单质氧化性的强弱:。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A是周期表中原子半径最小的元素;B的最高价氧化物的水化物与其氢化物能相互反应生成盐;A与C可形成两种液态化合物,其分子中电子总数分别为10和18;D元素的主族序数等于其周期数;E原子的最外层电子数是其电子层数的2倍。
(1)E元素在周期表中的位置是。
(2)A与C形成的18电子物质中所含的化学键类型是。
A.离子键B.极性共价键C.非极性共价键
(3)写出A和E形成的化合物在水中的电离方程式。
(4)实验室制备D的最高价氧化物的水化物的离子方程式为。
(5)B元素与C元素形成的化合物中,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的B的含氧酸盐的化学式是__________。
根据A—J在周期表中的位置,用元素符号或化学式回答下列问题: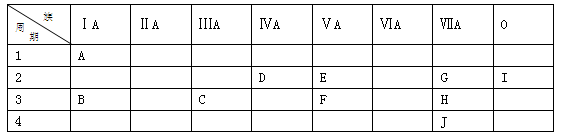
(1)J的原子结构示意图为。
(2)表中元素,化学性质最不活泼的是,只有负价而无正价的是,氧化性最
强的单质是,还原性最强的单质是。
(3)最高价氧化物的水化物碱性最强的是,酸性最强的是,呈两性的是。
(4)A分别与D、E、F形成的化合物中,最稳定的是。
(5)在C、D、G、H中,原子半径最大的是。