下列叙述正确的是
| A.分子式为C3H6有机物最多存在3个C—C单键,与C4H10的碳碳单键数相同 |
| B.乙烯、聚氯乙烯和苯分子中均含有碳碳双健 |
C.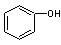 和 C7H8O分子组成相差一个—CH2—,因此是同系物关系 和 C7H8O分子组成相差一个—CH2—,因此是同系物关系 |
| D.分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可以确定有机物结构简式为C2H5-OH |
120°时,将1体积某气态烃与7体积氧气混合完全燃烧后恢复到原来的温度和压强时气体体积变为原来的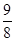 ,则该烃分子式不可能为
,则该烃分子式不可能为
| A.C3H8 | B.C4H8 | C.C5H8 | D.C7H8 |
设阿伏加德罗常数的值为NA,下列说法中正确的是
| A.2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| B.1mol 苯乙烯中含有的碳碳双键数为4NA |
| C.0.1mol CnH2n+2中含有的碳碳单键数为0.1n NA |
| D.标准状况下,2.24L CHCl3含有的分子数为0.1NA |
丙烯酸的结构简式为CH2=CH—COOH,其对应的性质中不正确的是
| A.与钠反应放出氢气 | B.与新制的Cu(OH)2悬浊液反应 |
| C.能与溴水发生取代反应 | D.发生相互加成反应生成高分子化 |
某气态烷烃与烯烃的混合气9 g,其密度为相同状况下氢气密度的11.25倍,将混合气体通过足量的溴水,溴水增重4.2 g,则原混合气体的组成为
| A.甲烷与乙烯 | B.甲烷与丙烯 | C.乙烷与乙烯 | D.甲烷与丁烯 |
分子组成为C4H90H并能发生催化氧化反应的有机化合物有
| A.2种 | B.4种 | C.5种 | D.3种 |