NA为阿伏加德罗常数,下列说法中正确的是
| A.标准状况下,22.4L CCl4中含有的CCl4分子数为NA |
| B.向FeI2溶液中通入适量Cl2,当有1 mol Fe2+被氧化时,共转移的电子的数目为NA |
| C.1.0 L 浓度为18mol·L-1H2SO4溶液与足量的铜片加热条件下反应,被还原的H2SO4的分子数为9NA |
| D.一定条件下,2.3gNa完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
还原2.4×10-3 mol [XO(OH)3]+ 到X元素的低价态时,消耗0.2mol·L—1的Na2SO3溶液30 mL,则X元素反应后的价态是()
| A.+1 | B.-1 | C.0 | D.-2 |
下列有关实验的说法正确的是()
| A.除去铁粉中混有少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤 |
| B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体后进行测量 |
| C.制各Fe(OH)3胶体,通常是将Fe(OH)3固体溶于热水中 |
| D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32— |
如图,B为常见金属或非金属单质,有下列转化关系
若C是可用作自来水消毒的气体,D、E是氧化物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,则A是( )
A.AlCl3B.H2O2C.KCl D.NaCl
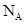 表示阿伏伽德罗常数,下列判断正确的是( )
表示阿伏伽德罗常数,下列判断正确的是( )
A.在18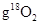 中含有NA个氧原子 中含有NA个氧原子 |
| B.标准状况下,22.4L空气含有NA个单质分子 |
| C.1 molCl2参加反应转移电子数一定为2NA |
D.含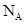 个 个 的 的 溶解于1L水中, 溶解于1L水中, 的物质的量浓度为1mol/L 的物质的量浓度为1mol/L |
下列反应的离子方程式不正确的是( )
| A.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+=4Fe3++2H2O |
| B.物质的量相等的溴化亚铁跟氯气反应 2Fe2+ + 2Br- + 2Cl2 = 2Fe3+ + Br2 + 4Cl- |
| C.向明矾溶液中滴加Ba(OH)2,恰好使SO42-沉淀完全:2A13++3SO42-+3Ba2++6OH-===2A1(OH)3 ↓ +3BaSO4 ↓ |
| D.向碳酸钠溶液中滴加过量的稀硫酸: CO32- + 2H+ = CO2↑+ H2O |