捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)  (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)  NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)  2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
请回答下列问题:
(1)ΔH3与ΔH1、ΔH2之间的关系是:ΔH3= 。
(2)反应Ⅲ的化学平衡常数表达式为 。
(3)为研究温度对(NH4)2CO3捕获CO2效率的影响,在某温度T1下,将一定量的(NH4)2CO3溶液置于密闭容器中,并充入一定量的CO2气体(用氮气作为稀释剂),在t时刻,测得容器中CO2气体的浓度。然后分别在温度为T2、T3、T4、T5下,保持其他初始实验条件不变,重复上述实验,经过相同时间测得CO2气体浓度,得到趋势图(见图1)。则:
①ΔH3 0(填“>”、“=”或“<”)。
②在T1~T2温度区间,容器内CO2气体浓度呈现如图1所示的变化趋势,其原因是
。
③反应Ⅲ在温度为T1时,溶液pH随时间变化的趋势曲线如图2所示。当时间到达t1时,将
该反应体系温度迅速上升到T2,并维持该温度。已知同浓度的(NH4)2CO3和NH4HCO3溶液
pH前者大,请在下图中画出t1时刻后溶液的pH变化总趋势曲线。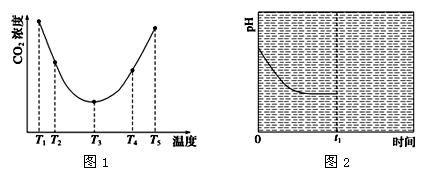
(4)利用反应Ⅲ捕获CO2,在(NH4)2CO3初始浓度和体积确定的情况下,提高CO2吸收量的措施有 。(答出一点即可)
(5)下列物质中也可以作为CO2捕获剂的是 。
A.NH4Cl B.Na2CO3 C.HOCH2CH2OH
现有A、B两种烃,已知A的分子式为C5Hm,而B的最简式为C5Hm(m、n均为正整数)。
(1)下列关于烃A和烃B的说法中不正确的是____(填字母编号)
a.烃A和烃B可能互为同系物
b.烃A和烃B可能互为同分异构体
c.当m=12时,烃A-定为烷烃
d.当n=11时,烃B可能的分子式有两种
e.烃A和烃B可能都为芳香烃
(2)若烃A为链状烃,且分子中所有碳原子都在一条直线上,则A的结构简式为。
(3)若烃A为链状烃,分子中所有碳原子不可能都在同一平面上。在一定条件下,1mol A最多只能与1mol H2发生加成反应。写出烃A的名称。
(4)若烃B为苯的同系物,取一定量的烃B完全燃烧后,生成物先通过足量浓硫酸,浓硫酸增重1. 26g,再通过足量碱石灰,碱石灰增重4.4g,则烃B的分子式为。若其苯环上的一溴代物只有一种,则符合条件的烃B有种。
(5)当m= n=4时,取A和B组成的混合物ag完全燃烧后,将产物通过足量Na2O2固体充分吸收,固体增重g(用含a的代数式表示)。
在一个容积固定为2L的密闭容器中,发生反应 △H=?。反应情况记录如下表:
△H=?。反应情况记录如下表:
| 时间 |
c(A)/mol  L-1 L-1 |
c(B)/mol L-1 |
c(C)/mol L-1 |
| 0min |
1 |
3 |
0 |
第2m in in |
0.8 |
2.6 |
0.4 |
| 第4min |
0.4 |
1.8 |
1.2 |
| 第6min |
0.4 |
1.8 |
1.2 |
| 第8min |
0.1 |
2.0 |
1.8 |
| 第9min |
0.05 |
1.9 |
0.3 |
请仔细分析根据表中数据,回答下列问题:
(1)a2=,b=,p=。(取最小正整数)
(2)第2min到第4min内A的平均反应速率v(A)=mol·L-1·min-1[来源:学.科.网]
(3)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、第6min、第8min时分别改变了某一反应条件,则改变的条件分别可能是:
①第2min 或
②第6min;
③第8min;
(4)若从开始到第4min建立平衡时反应放出的热量为235。92kJ,则该反应的△H=。
已知A、B、C、D、E为中学常见的五种物质,均含元素Y,有的还可能含有元素X、Z,元素X、Y、Z的原子序数依次递增。①元素Y在A、B、C、D、E中所呈化合价依次递增,其中只有B为单质。②常温下将气体D通入水中发生反应,生成C和E;③工业上以A、空气和水为原料,通过催化氧化法制取E。请回答以下问题:
⑴ B分子中含有的化学键为;A的分子式为;
(2)由B反应生成1molA放出的热量为46.2kJ,写出该反应的热化学方程式
将某一元酸HA与NaOH等体积混合,请根据题目要求回答下列问题:
(1)若c(HA)=c(NaOH)=O.lmol/L,测得混合后溶液的pH>7。
①HA是弱电解质,能证明HA是弱电解质的方法是()。
A测得0. Imol/L HA的pH>l B.测得NaA溶液的pH>7
C.pH=l的HA与盐酸,稀释10倍后,盐酸的pH变化大
D.用足量的锌分别与相同pH、相同体积的盐酸和HA反应,产生氢气一样多
②混合溶液中,关系式一定正确的是( )。
A.c(A-)>c(Na+)c(OH-)>c(H+)B.c(A-)+c(OH-)=c(Na+)+c(H+)
C.c(HA)+c(A-)=0.1mol/L D.C( HA) +c( H+)= c(OH-)
③若HA(足量)+B2一A一+HB-;H2B(少量)+2C-B2-+2HC: HA+C-A-十HC
则相同pH的①NaA②Na2B③NaHB④NaC的四种溶液,各物质的物质的量浓度从大到小的顺序为
(填序号)。
(2)若c( HA)==c(NaOH)==0.1mol/L,测得混合后溶液的pH=7。
①现将一定浓度的HA稀释10倍后溶液的pH与该浓度的HA和0.1 mol/L NaOH等体积混合后溶液的pH相等,则HA溶液的浓度为。
②用标准的NaOH溶液滴定未知浓度的HA时,下列操作能引起所测HA浓度偏低的是。
A.用蒸馏水洗涤锥形瓶后,用待测HA溶液进行润洗
B.滴定前发现滴定管的尖嘴部分有气泡,滴定后消失
C.装NaOH的碱式滴定管未用标准的NaOH溶液润洗
D.滴定前仰视,滴定后俯视读数
对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:
①碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出,原因是______(用离子方程式表示)。为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的_______________。
a.NH3 b.CO2c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应为_______________。取少量废电解液,加入NaHCO3,溶液后产生气泡和白色沉淀,产生沉淀的原因(用离子方程式表示)___________________________。
(2)利用如图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于______处。
若X为锌,开关K置于M处,该电化学防护法称为_______。