电解熔融氯化钙可以得到金属钙和氯气,钙在氯气中燃烧又能生成氯化钙.请你根据已学知识,按如图箭头所表示的物质间可能发生的转化,分析下列说法中正确的是
| A.CaO、Ca(OH)2、CaCO3都含有氧元素,所以CaO、Ca(OH)2、CaCO3都属于氧化物 |
| B.电解熔融氯化钙得到金属钙和氯气的反应既是氧化还原反应又是化合反应 |
| C.虽然碳酸钙的水溶液不导电,但碳酸钙是电解质 |
| D.工业上以氯气和石灰水为原料通过反应④生产漂白粉 |
下列关于有机物说法不正确的是()
| A.2,2-二甲基丙醇和2-甲基-1-丁醇互称为同分异构 |
| B.沸点比较:乙醇>丙烷>乙烷 |
C.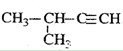 命名为3-甲基-1-丁炔 命名为3-甲基-1-丁炔 |
| D.含5个碳原子的有机物,每个分子中最多可形成4个C-C单键 |
在室温下,下列叙述正确的是()
| A.将1 mL 1.0×10-5 mol/L盐酸稀释到1000 mL,得到pH=8 的盐酸 |
| B.将1 mL pH=3的一元酸溶液稀释到10 mL,若溶液的pH<4,则此酸为弱酸 |
| C.用pH=1的盐酸分别中和1 mL pH="13" NaOH溶液和氨水,NaOH消耗盐酸的体积大 |
| D.pH=2的盐酸与pH=1的硫酸比较,2 c(Cl— )=c(SO42— ) |
下列有关实验操作不正确的是 ()
| A.中和热的测定实验中用到的玻璃仪器有温度计、烧杯、环形玻璃搅拌棒 |
| B.滴定管在使用前必须检验是否漏水 |
| C.某次滴定后滴定管的读数为20.3ml |
| D.碱式滴定管不能量取盐酸的体积 |
25 ℃时,水的电离达到平衡:H2O H++OH-;ΔH>0,下列叙述正确的是()
H++OH-;ΔH>0,下列叙述正确的是()
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热, Kw增大,pH不变 |
下列有关说法不正确的是( )
| A.CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△S<0 |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
C.N2(g)+3H2(g) 2NH3(g) △H<0,其他条件不变时升高温度,反应速率V(H2)和 2NH3(g) △H<0,其他条件不变时升高温度,反应速率V(H2)和V(NH3)均增大 |
| D.水的离子积常数Kw随着温度的升高而增大,说明水的电离是吸热反应 |