常温下,下列溶液中有关物质的量浓度关系和计算不正确的是
A.c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4C1溶液中,溶质物质的量浓度大小关系是: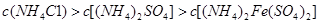
B.已知25℃时Ksp(AgCl)=1.8×10-10,则在0.1 mol·L-l A1Cl3溶液中,Ag+的物质的量浓度最大可达到6.0×10-10 mol·L-l
C.25℃时0.2 mol·L-l HC1溶液与等体积0.05 mol·L-l Ba(OH)2溶液混合后,溶液的pH约为1
D.0.1mol·L-l NaHA溶液的pH=4,则有c(HA-)>c(H+)>c(A2-)>c(H2A)
有①Na2CO3溶液;②CH3COONa溶液;③NaOH溶液各25mL,物质的量浓度均为0.1mol/L,下列说法正确的是( )
)
| A.3种溶液pH的大小顺序是 ③>②>① |
| B.若将3种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25mL0.1mol·L-1盐酸后,pH最大的是① |
| D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>①>② |
在100 mL某一元弱酸(HA)的溶液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示,下列叙述正确的是( )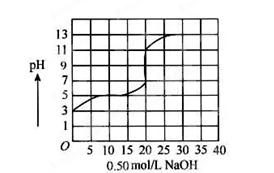
A.该弱酸在滴定前的浓度是0.15 mol/L
B.该弱酸稀释10倍后pH为4
C.滴定过程为求滴定终点,最合适的指示剂是酚酞
D.滴定终点时,c(A-)=c(Na+)>c(H+)=c(OH-)
甲酸和乙酸都是弱酸,当他们的浓度均为0.1 0mol/L时,甲酸中的氢离子浓度约为乙酸中的氢离子浓度的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10mol/L的乙酸,经测定它们的pH从大到小依次为a、乙酸、
0mol/L时,甲酸中的氢离子浓度约为乙酸中的氢离子浓度的3倍。现有两种浓度不等的甲酸溶液a和b,以及0.10mol/L的乙酸,经测定它们的pH从大到小依次为a、乙酸、 b。由此可知()
b。由此可知()
A.a的浓度必小于乙酸的浓度 B.a的浓度必大于乙酸的浓度
下列事实可以证明一水合氨是弱电解质的是( )
①0.1 mol/L的氨水可以使酚酞溶液变红
②0.1 mol/L的氯化铵溶液的pH约为5
③在相同条件下,氨水溶液的导电性比一元强碱溶液弱
④铵盐受热易分解
| A.①② | B.②③ | C.③④ | D.②④ |
下列叙述中,错误的是( )
| A.虽然固体氯化钠不能导电,但氯化钠是电解质 |
| B.纯水的pH随温度的升高而减小 |
| C.在醋酸钠溶液中加入少量氢氧化钠,溶液中c(OH-)增大 |
| D.在纯水中加入少量硫酸铵,可抑制水的电离 |