在温度T ℃下,某Ba(OH)2稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,向该溶液中逐滴加入NaHSO4溶液,测得混合溶液的部分pH如下表所示:
| 序号 |
氢氧化钡的体积/mL |
硫酸氢钠的体积/mL |
溶液的PH |
| ① |
33.00 |
0.00 |
8 |
| ② |
33.00 |
X |
7 |
| ③ |
33.00 |
33.00 |
6 |
(1)依据题意判断,T ℃________25 ℃(填“大于”、“小于”或“等于”);
(2)b= ,X= ;
(3)反应③的离子方程式为: ;
(4)将此温度下的Ba(OH)2溶液取出1 mL,加水稀释至1L,则稀释后溶液中c(Ba2+):c(OH-) 。
(1)写出下图中序号①~③仪器的名称:
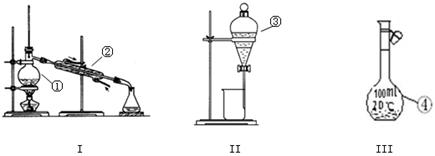
①;②;③。
(2)仪器①~④中,使用时必须检查是否漏水的有 。(填仪器序号)
(3)下图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。
现用该浓硫酸配制480 mL 1 mol· L-1的稀硫酸。
可供选用的仪器有:①胶头滴管②烧瓶③烧杯④ 玻璃棒⑤药匙⑥量筒⑦托盘天平。
请回答下列问题:
a.该硫酸的物质的量浓度为mol· L-1。
b.配制稀硫酸时,还缺少的仪器有 (写仪器名称)。
c.经计算,配制480mL 1mol· L-1的稀硫酸需要用量筒量取上述浓硫酸的体积为__mL。
d.对所配制的稀硫酸进行测定,发现其浓度大于1 mol· L-1,配制过程中下列各项操作可能引起该误差的原因有。
| A.定容时,俯视容量瓶刻度线进行定容 。 |
| B.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作。 |
| C.转移溶液时,不慎有少量溶液洒到容量瓶外面。 |
| D.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水 。 |
E.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处。
火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+3C+S===K2S+N2↑+3CO2↑。
(1)其中被还原的元素是
(2)当反应有3.612×1024个电子转移时被硝酸钾氧化得到的氧化产物在标准状况下的体积。
(10)按要求填空
(1)金属钠与水反应的化学方程式:
(2)金属铝与氢氧化钾反应的离子方程式:
(3)硫酸氢钠与少量的氢氧化钡反应的离子方程式:
(4)Na+的原子结构示意图:
(5)标准状况下11.2L N2含有的原子数:
(6)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则A的摩尔质量是___
【化学——选修5:有机化学基础】
A、B、C、D、E、F都是链状有机物,它们的转化关系如图所示。A中只含有一种官能团,D中含有两种官能团,D分子中不含甲基,且与碳原子相连的氢原子取代所得的一氯代物只有一种。请回答下列问题: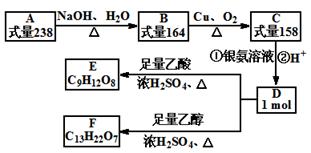
(1)A中含有的官能团是。
(2)请写出B生成C的化学方程式。
(3)写出C与银氨溶液反应的化学方程式。
(4)请考虑满足下列条件的E的同分异构体有种
①遇FeCl3溶液显紫色;②含有3个-CH2OH结构;③不含有“-O-O-”这样不稳定的结构
【化学—选修3物质结构与性质】(14分)
现有X、Y、Z、W原子序数依次增大的四种元素,常温下X元素单质的密度在自然界中最小,Y是短周期元素中未成对电子数与原子序数之比最大的原子,Z元素基态原子的核外电子排布式中,s亚层电子总数与p亚层电子总数相等,且Y与Z可形成多种气态化合物,W是常见的有色可变价金属单质,常温下可溶于Y的最高价氧化物水化物中,其基态原子的内层轨道全部排满电子,且最外层电子数为1。
(1)Y与W所形成化合物晶体的晶胞如图所示。在1个晶胞中,W离子的数目为。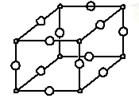
(2)在Y与X形成的分子中,Y原子轨道的杂化类型是。
(3)X与Y形成的气态物质在X与Z形成的气态物质中有很大的溶解度,其原因是存在氢键,若在两种氢化物的混合溶液中,再滴加少量的乙醇,则分子间存在种不同类型的氢键。
(4)Y与Z可形成化合物Y2Z。
①请写出一种与Y2Z互为等电子体的分子的化学式。
②请预测Y2Z分子的空间构型为。
(5)Y与Z元素相比,基态原子的第一电离能谁大?(用元素名称回答)。
(6)X的氯化物与Y元素的气态氢化物的水溶液反应可形成配合物[W(YX3)4]Cl2,1 mol该配合物中含有σ键的数目为个。