在一定体积的密闭容器中放入3升气体R和5升气体Q,在一定条件下发生反应:2R(g)+5Q(g)
4X(g)+nY(g)。反应完全后,容器温度不变,混和气体的压强是原来的87.5%,则化学方程式中的n值是
| A.2 | B.3 | C.4 | D.5 |
质量相同的Na、Mg、Al、Zn分别放入足量的稀盐酸中,在相同的条件下,产生氢气最多的是
| A.Na | B.Mg | C.Al | D.Zn |
阿波罗宇宙飞船以N2H4(联氨)和N2O4为动力源,反应温度达2700℃,反应方程式为:2N2H4+N2O4=3N2+4H2O,关于该反应的说法中正确的是
| A.属于置换反应 | B.联氨是氧化剂 |
| C.联氨是还原剂 | D.氮气是氧化剂,不是还原剂 |
下列反应不属于四种基本反应类型,但属于氧化还原反应的是
| A.2F2+2H2O=4HF+O2↑ |
B.CO+ FeO Fe+ CO2 Fe+ CO2 |
| C.2AgNO3+Na2CO3=2NaNO3+Ag2CO3↓ |
D.2Cu(NO3)2 2CuO+ 4NO2↑+O2↑ 2CuO+ 4NO2↑+O2↑ |
符合图中阴影部分的物质是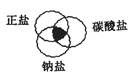
| A.Na2CO3 | B.Cu2(OH)2CO3 | C.NaCl | D.NaHCO3 |
下列有关胶体的说法正确的是
| A.胶体都是均匀透明的液体 |
| B.直径介于1nm~100nm之间的微粒称为胶体 |
| C.胶体与溶液有明显不同的外观特征,呈胶状 |
| D.利用丁达尔效应可区别溶液和胶体 |