某强酸性溶液X中含有Ba2+、Al3+、SiO32-、NH4+、Fe2+、Fe3+、CO32-、SO42-、NO3-中的一种或几种离子,取该溶液进行连续实验,能实现如下转化:根据以上信息,判断下列说法错误的是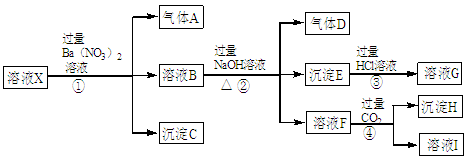
| A.溶液X中除H+外肯定含有的离子是:SO42—、Al3+、NH4+、Fe2+ |
| B.沉淀E的化学式为Fe(OH)3 |
| C.不能确定是否含有的离子是NO3— |
| D.反应①、②、③、④中,属于氧化还原反应的是① |
下列叙述错误的是
| A.用金属钠可区分乙醇和乙醚 |
| B.用高锰酸钾酸性溶液可区分己烷和3-己烯 |
| C.用水可区分苯和溴苯 |
| D.用新制的银氨溶液可区分甲酸甲酯和乙醛 |
分子式为C5H11Cl的同分异构体共有(不考虑立体异构)
| A.9种 | B.8种 | C.7种 | D.6种 |
将有机物完全燃烧,生成CO2和H2O,将12 g该有机物完全燃烧产物通过浓硫酸,浓硫酸增重14.4 g,再通过碱石灰,又增重26.4 g。则该有机物的分子式为
| A.C4H10 | B.C2H6O | C.C3H8O | D.C2H4O2 |
下列化合物分子中,在核磁共振氢谱图中能给出三种信号的是
| A.CH3CH2CH3 | B.CH3CH2COCH2CH3 | C.CH3CH2OH | D.CH3OCH3 |
仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式 是
是
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
…… |
| C2H2 |
C2H4 |
C2H6 |
C3H4 |
C3H6 |
C3H8 |
C4H6 |
C4H8 |
C4H10 |
…… |
A.C6H12 B.C6H14 C.C7H12 D.C7H14