研究表明丰富的CO2完全可以作为新碳源,解决当前应用最广泛的碳源(石油和天然气)到本世纪中叶将枯竭的危机,同时又可缓解由CO2累积所产生的温室效应,实现CO2的良性循环。
(1)目前工业上有一种方法是用CO2和H2在230℃催化剂条件下转化生成甲醇蒸汽和水蒸气。下图表示恒压容器中0.5 mol CO2和1.5 mol H2转化率达80%时的能量变化示意图。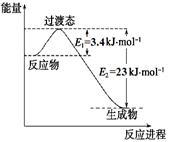
①写出该反应的热化学方程式:_______________________。
②能判断该反应达到化学平衡状态的依据是_____。
a.容器中压强不变
b.H2的体积分数不变
c.c(H2)=3c(CH3OH)
d.容器中密度不变
e.2个C=O断裂的同时有6个H-H断裂。
(2)最近有科学家提出构想:把空气吹入饱和碳酸钾溶液,然后再把CO2从溶液中提取出来,经化学反应后使之变为可再生燃料甲醇。该构想技术流程如下: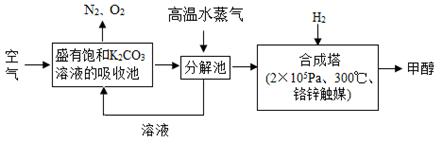
①向分解池中通入高温水蒸气的作用是________。
②甲醇可制作燃料电池,写出以稀硫酸为电解质甲醇燃料电池负极反应式_________。当电子转移的物质的量为________时,参加反应的氧气的体积是6.72L(标准状况下)。
(3)某国科研人员提出了使用氢气和汽油(汽油化学式用C8H18表示)混合燃料的方案,以解决汽车CO2的排放问题。该方案主要利用储氢材料CaH2产生H2和用汽油箱贮存汽油供发动机使用,储氢系统又捕集汽油燃烧产生的CO2,该系统反应如下图所示: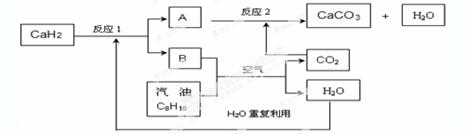
解决如下问题:①写出CaH2的电子式______________________。
②反应1中氧化剂与还原剂的物质的量之比是:____________。
③如该系统反应均进行完全,试写出该系统总反应的化学方程式________________。
某化学反应2A B+D在四种不同条件下进行。B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行。B、D起始浓度为0。反应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验序号 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
|
| 1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800℃ |
c2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
800℃ |
c3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
| 4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20分钟内平均速率为。
(2)在实验2中,A的初始浓度c2=__________,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是__________。
(3)设实验3中的反应速率为v3,实验1的反应速率为v1,则v3__________v1(填“>”、“=”或“<”),且c3__________1.0mol·L-1(填“<”、“=”或“>”)。
(4)比较实验4和实验1,可推测该反应是__________反应(填“吸热”或“放热”)。
发展混合动力车是实施节能减排的重要措施之一。混合动力车可以用电动机、内燃机或二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗。
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1mol水蒸气放热569.1kJ。则该反应的热化学方程式为。
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液。镍氢电池充放电原理如下图,其总反应式是:
H2+2NiOOH 2Ni(OH)2。
2Ni(OH)2。
根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将
(填“增大”、“不变”或“减小”),该电极的电极反应式为;在刹车和下坡时甲电极的电极反应为。
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:
(g)。已知:平衡时各物质的浓度关系有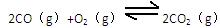
已知:平衡时各物质的浓度关系有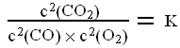 ,K是一个只与温度有关的常数,称为化学平衡常数。
,K是一个只与温度有关的常数,称为化学平衡常数。
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示。请填写表中的空格。
| 容器编 号 |
c(CO)/ mol/L |
c(O2)/ mol/L |
c(CO2)/ mol/L |
v(正)和v(逆)的比较 |
| Ⅰ |
2.0×10-4 |
4.0×10-4 |
4.0×10-2 |
v(正)= v(逆) |
| Ⅱ |
3.0×10-4 |
4.0×10-4 |
5.0×10-2 |
②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5 mol/L和1.0×10-4mol/L。若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4mol/L,则最终尾气中CO的浓度为。
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂
中铁元素的含量。实验步骤如下: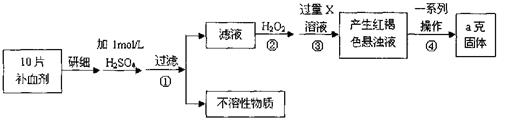
请回答下列问题:
(1)步骤②加入过量H2O2的目的:
(2)步骤③中反应的离子方程式:
(3)步骤④中一系列处理的操作步骤:过滤、、灼烧、、称量。
(4)若实验过程中无损耗,则每片补血剂含铁元素的质量g(用含a的代数式表示)。
(5)该小组有些同学认为用KMnO4溶液滴定也能进行铁元素含量的测定。
(5Fe2++MnO4—+8H+= 5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需
②某同学设计的下列滴定方式中,最合理的是(夹持部分略去)(填字
母序号) 
(6)正常人每天应补充14mg左右的铁。其中绝大部分来自于食物。如果全部通过服用
含FeSO4·7H2O的片剂来补充铁,则正常人每天需服用含mgFeSO4·7H2O的
片剂。
A、D、E、X、Y五种短周期元素,它们的原子序数依次增大,A元素的原子
是半径最小的原子,D元素的最高价氧化物对应的水化物与其氢化物反应生成一种盐;X与A同主族;Y元素的最外层电子数是其次外层电子数的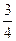 倍;A、D、X、Y四种元素,每一种均能与E元素形成原子个数比不相同的若干化合物。
倍;A、D、X、Y四种元素,每一种均能与E元素形成原子个数比不相同的若干化合物。
(1)画出Y元素离子的结构示意图;写出常温下Y的氢化物与其最高价氧化物对应水化物的浓溶液反应的化学方程式。
(2)由A、D、E、Y四种元素形成的强酸的酸式盐的名称为,该盐的水溶液中各离子浓度由大到小的顺序为。
(3)科学家用D、E、X 三种元素形成的化合物XDE3和X2E,在573K时反应制得了离子化合物X3DE4;经测定X3DE4中各原子的最外层电子都达到了8电子稳定结构,则DE43-的电子式为,X3DE4与水能剧烈反应转化为常见物质,写出反应的化学方程式:。
现有浓度均为0.1 mol/L的下列溶液:①硫酸 ②醋酸 ③氢氧化钠
④氯化铵 ⑤醋酸铵 ⑥硫酸铵 ⑦硫酸氢铵 ⑧氨水,请回答下列问题:
(1)①②③④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)_。
(2)④⑤⑥⑦⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)___ ___。 (3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是 _____。
(3)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是 _____。
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”)25℃。在t℃时将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=。
(5)25℃时,有pH=x的盐酸和pH="y" 的氢氧化钠溶液(x≤6,y≥8),取aL该盐酸与该氢氧化钠溶液中和,消耗bL的氢氧化钠溶液,问:
①若x+y=14,则a/b=____(填数据);②若x+y=13,则a/b=____
(填数据);
③若x+y>14,则a/b=____(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的pH x和y的关系式(填表达式)。