既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯的方法是
| A.通入足量溴水中 | B.在空气中燃烧 |
| C.通入酸性高锰酸钾溶液中 | D.在一定条件下通入氢气 |
下列关于稀有气体的叙述中,不正确的是()
A.原子的最外电子层都有8个电子
B.其原子与同周期ⅥA、ⅦA族元素形成的阴离子具有相同的核外电子排布
C.通常条件下,化学性质非常不活泼
D.原子核外电子的排布都达到了稳定结构
在2A+B=3C+4D反应中,表示该反应速率最快的数据是()
| A.υA= 0.5mol/(L·s) | B.υB= 0.3mol/(L·s) |
| C.υC= 0.8mol/(L·s) | D.υD= 1.0mol/(L·s) |
今年央视“315特别行动”又曝光了河南一些地方“瘦肉精”事件。“瘦肉精”对人体健康会产生危害。已知某中“瘦肉精”含有克伦特罗(Clenbuterol),其结构如图。下列有关克伦特罗的叙述,不正确的是
| A.该物质的分子式为C12H18ON2Cl2 |
| B.该物质可与盐酸反应 |
| C.该物质的核磁共振氢谱图中有8个吸收峰 |
| D.该物质能发生的类型有:加成反应、酯化反应、消去反应、氧化反应等 |
分子式为C4H8O3的有机物在一定条件下具有如下性质:
①在浓硫酸存在下,能与CH3CH2OH、CH3COOH反应
②在浓硫酸存在下,能脱水生成一种能使溴水褪色的物质,该物质只存在一种结构
③在浓硫酸存在下,能生成一种分子式为C4H6O2的五元环状化合物
则C4H8O3的结构简式为( )
| A.HOCH2COOCH2CH3 | B.CH3CH(OH)CH2COOH |
| C.HOCH2CH2CH2COOH | D.CH3CH2CH(OH)COOH |
市场上销售的强生、妙思乐及帮宝适等婴儿卫浴产品常常标有“温和”、“纯净”等字样,但其中却含有甲醛以及1,4-二氧杂环乙烷等有害物质。1,4-二氧杂环乙烷的结构简式为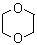 ,下列有关其性质的叙述正确的()
,下列有关其性质的叙述正确的()
| A.1,4-二氧杂环乙烷与丁酸互为同分异构体 |
| B.1,4-二氧杂环乙烷与乙酸乙酯互为同系物 |
| C.1,4-二氧杂环乙烷与钠反应可放出氢气 |
| D.1,4-二氧杂环乙烷的分子间可形成氢键 |