已知:①Na3N+3H2O===3NaOH+NH3↑,②NaH+H2O===NaOH+H2↑下列叙述正确的是
| A.离子半径:N3->Na+>H+ |
| B.反应①和②都是氧化还原反应 |
| C.反应①和②氧化剂都是H2O |
| D.Na3N和NaH与盐酸反应都只生成一种盐 |
下列实验步骤与实验事实的相应结论解释正确的是
| 选项 |
实验步骤与实验事实 |
结论解释 |
| A |
Mg(OH)2、Al(OH)3混合物中加入NaOH溶液,Al(OH)3溶解而Mg(OH)2没有溶解 |
Mg(OH)2Ksp比Al(OH)3的小 |
| B |
ZnS能溶解在稀盐酸中,CuS不能溶解在稀盐酸中 |
CuS的Ksp比ZnS的小 |
| C |
在溶有NH3的BaCl2溶液中通入CO2,有白色沉淀生成 |
NH3在反应中作催化剂 |
| D |
单质硅不溶于浓硫酸和浓硝酸 |
硅被强氧化性酸钝化 |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是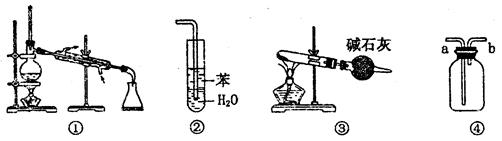
| A.装置①常用于分离沸点不同的液体混合物 |
| B.装置②用于吸收氨气,能够防止倒吸 |
| C.以NH4Cl为原料,装置③可制备少量NH3 |
| D.装置④从a口进气可收集Cl2、NO等气体 |
下列叙述中正确的是
| A.加入NaOH溶液,加热后产生气体使湿润的红色石蕊试纸变蓝,则原溶液一定有NH4+ |
| B.能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
| C.加入盐酸酸化的BaCl2溶液,有白色沉淀生成,则原溶液一定有SO42- |
| D.加盐酸生成的气体能使澄清石灰水变浑浊,则原溶液中一定含有CO32- |
可逆反应A(?)+a B(g) C(g)+2 D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列说法不正确的是
C(g)+2 D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列说法不正确的是
| A.当压强由p1变为 p2时,逆反应速率将变大 |
| B.该反应的正反应为放热反应 |
| C.若a=2,则A为液态或固体 |
| D.恒温恒容条件下,增加B的物质的量,B的转化率和该反应的化学平衡常数都将增大 |
用下图所示的装置制取、提纯并收集表中的四种气体,图中a、b、c表示相应仪器加入的试剂,未考虑尾气处理的问题,其中可行的是
| 气体 |
a |
b |
C |
|
| A |
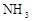 |
浓氨水 |
生石灰 |
碱石灰 |
| B |
 |
稀硝酸 |
铜片 |
碱石灰 |
| C |
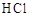 |
浓硫酸 |
浓盐酸 |
氯化钙 |
| D |
SO2 |
浓硫酸 |
铜片 |
硅胶 |