有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、NaCl等混合组成,为了检验它们所含的物质,做了以下实验: ①将固体溶于水,搅拌后得到无色透明溶液;
②往此溶液中滴加硝酸钡溶液,有白色沉淀生成;
③过滤,将沉淀置于稀硝酸中,发现沉淀全部溶解。
(1)试判断:固体混合物中肯定含有 ,肯定没有 ;
(2)对可能有的物质,可采用往滤液中滴加 (填试剂名称)来检验;
(3)写出③中涉及的化学方程式 。
电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题: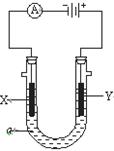
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
①电解池中X极上的电极反应式为。
在X极附近观察到的现象是。
② Y电极上的电极反应式为,检验该电极反应产物的方法是。
下表是元素周期表的一部分:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
① |
② |
||||||
| 3 |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
||
| 4 |
⑨ |
⑩ |
(1)表中元素⑦的氢化物的化学式为,此氢化物的还原性比元素⑩的氢化物的还原性(填强或弱)
(2)某元素原子的M层 p电子数比s电子数少1,则该元素的元素符号是,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的离子方程式:
_________________________________________________________________________;
_________________________________________________________________________;
(3)③④⑤的第一电离能由大到小的顺序____________(写元素符号)
(4)表格中电负性最大的元素______,电负性最小的元素_____(写元素符号)
(19分)原电池是将能转化为能的装置,一般较活泼的金属做极,发生反应,如: 锌,铜和稀硫酸构成的原电池,锌是极,反应方程式是 ;铜是极, 反应方程式是,总反应方程式是.
(21分) 现有A、B、C、D、E五种短周期元素,它们的核电荷数依次增大。①A是原子半径最小的元素;② B2是大气中含量最多的气体,它与A可形成10电子的分子; ③C与A形成的化合物在常温下为液体,该物质也是10电子的分子④D可形成正1价离子D+, D单质与冷水剧烈反应放出氢气,且D的焰色反应呈黄色;⑤ E和D两种元素可形成离子化合物DE,该化合物的溶液中加入硝酸酸化的A gNO3溶液产生白色沉淀..
(1) 写出下列元素的符号: A; B;C ; D;E。
(2) 写出A与B,A与C形成的10电子分子的化学式:;。
(3) 写出A与C形成的10电子分子的电子式: .
(4) 用电子式表示DE的形成过程:
(5) 写出D与水反应的化学方程式:;
(12分)写出Na和S的原子结构示意图:,.指出Na和S在元素周期表中的位置,Na: , S:.