密闭容器中mA(g)+nB(g)  pC(g),反应达到平衡,经测定增大压强P时,
pC(g),反应达到平衡,经测定增大压强P时,
A的转化率随P而变化的曲线如图。
则:(1)增大压强:A的转化率 ,平衡向 移动,达到平衡后,混合物中C的质量分数_____ 。
(2)上述化学方程式中的系数m、n、p的正确关系是 。
(3)降低温度,C的质量分数增大,则:平衡向 移动,A的转化率 ,正反应是 热反应。(以上各空用适当的化学用语或关系式填写)
甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。
(1)101 kPa时,1 mol CH3OH完全燃烧生成稳定的氧化物放出热量726.51 kJ,则甲醇燃烧的热化学方程式为。
(2)甲醇燃料电池的结构示意图如下左图。甲醇进入极(填“正”或“负”),正极发生的电极反应为。
(3)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验。在体积为1L的密闭容器中,充入1molCO2和3molH2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H =-49.0KJ/mol
CH3OH(g)+H2O(g)△H =-49.0KJ/mol
测得CO2和CH3OH(g)的浓度随时间变化如上右图所示。
①从反应开始到平衡,氢气的平均反应速率v(H2)=
②该反应的平衡常数表达式为。
③下列措施中能使n(CH3OH)/n(CO2)增大的是。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1molCO2和3molH2
短周期元素形成的纯净物A、B、C、D、E是转化关系如下图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同)。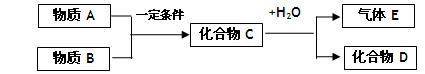
请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的一种化学式。
(2)若E的水溶液呈现弱酸性,D是既能溶于强酸、又能溶于强碱的化合物。
①用电离方程式解释D既能溶于强酸,又能溶于强碱的原因。
。
②用等式表示E与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系
。
(3)若C是一种气体,D是一种强酸,则:
①C与水反应的化学方程式为。
②有人认为“浓H2SO4可以干燥气体C”。某同学为了验证该观点是否正确,用下图装置进行实验。实验过程中,浓H2SO4中未发现有气体逸出,且变为红棕色,则你得出的结论是。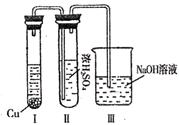
③已知常温下物质A与物质B生成1mol气体C的△H为-57.07kJ·mol-1,1 mol气体C与H2O反应生成D溶液和E气体的△H为-46kJ ·mol-1,写出物质A与物质B及水生成D溶液的热化学方程式。
(1)金属钠着火,_________(填“能”或“不能”)用水灭火,原因是________________________________________________________(用化学反应方程试解释);______(填“能”或“不能”)用泡沫灭火器灭火,原因是____________________________(用化学反应方程试解释)。
(2)甲型H1N1流感病毒在全球广泛传播,给人类健康、社会经济带来了巨大的负面影响。我国采取积极应对措施,使病毒得到了有效控制,从很大程度上减少了损失,在这里,消毒液功不可没。①生产消毒液是将氯气通入NaOH溶液中,发生的离子反应方程式为_____________________________________。
②消毒液稀释后喷洒在空气中,可以生成有漂白性的物质,请写出此过程的离子反应方程式_____________________________________;该物质有漂白性是因为它有强氧化性,但是它很不稳定,请写出它分解的化学方程式_____________________________________。
(1)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+ 转变为易吸收的Fe2+,,这说明维生素C具有[(填“氧化性”或“还原性”)
(2)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时的反应为:S+2KNO3 +3C=K2S+N2↑+3CO2↑.该反应中还原剂是,氧化剂是。
+3C=K2S+N2↑+3CO2↑.该反应中还原剂是,氧化剂是。
有一包粉末状固体,可能是由Al2(SO4)3、CuCl2、KNO3、Na2O中的一种或几种组成的。为了探究它的成分,某学习小组做了如下实验。
①取适量粉末投入蒸馏水中,粉末完全溶解,得到蓝色透明溶液A。
②取A溶液少量,向其中逐滴滴加烧碱溶液直到过量,观察到先有沉淀出现,而后沉淀逐渐增多,然后沉淀又逐渐减少,但最终仍有部分蓝色沉淀。
③再取A溶液两份,一份滴加BaCl2溶液后,出现白色沉淀;另一份滴加硝酸银溶液后也出现白色沉淀。请回答下列问题:
(1)原白色粉末一定含有 ,一定不含,可能含有。(填化学式)
,一定不含,可能含有。(填化学式)
(2)写出过程②中涉及到的离子方程式: 。
。
(3)如果要进一步确定可能存在的物质,进行的实验操作及实验现象和结论是
。